Spis treści
Burza cytokinowa – co to jest?
Burza cytokinowa, inaczej hipercytokinemia lub kaskada cytokin, jest nadmierną i niekontrolowaną reakcją układu odpornościowego, który uwalniania ogromne ilości substancji prozapalnych. Nieleczona burza cytokinowa może prowadzić do poważnych powikłań takich jak sepsa, wstrząs, uszkodzenia tkanek i niewydolność wielu narządów, a w następstwie śmierć.
Burza cytokinowa nie jest klasyfikowana jako jednostka chorobowa, ale jako zespół reakcji odpornościowych, który może pojawić się w przebiegu różnych stanów klinicznych np. chorób zakaźnych.
Termin „burza cytokinowa” został po raz pierwszy użyty w 1993 roku aby opisać skutki choroby przeszczep przeciwko gospodarzowi, który może pojawić się w organizmie biorcy po przeszczepieniu narządów. W 2003 roku wykazano również, że burza cytokinowa może być związana z reakcją organizmu na zakażenia wirusami, bakteriami lub grzybami.
Termin „burza cytokinowa” wydaje się po raz pierwszy użyty w kontekście zakażenia wirusem ptasiej grypy H5N1 w 2005 roku. Wtedy zaczął on być stosowany coraz powszechniej w literaturze naukowej.
Burza cytokinowa – mechanizm powstawania
Do zainicjowania burzy cytokinowej może dojść np. w trakcie zakażenia wirusem grypy. Po zakażeniu wirus wnika do komórek nabłonkowych górnych i dolnych dróg oddechowych poprzez proces endocytozy. Następnie wirusowy materiał genetyczny zostaje rozpoznany przez tzw. wzorce molekularne związane z patogenem (w skrócie PAMP), które z kolei mogą inicjować odpowiedź układu odpornościowego, w tym burzę cytokinową.
W trakcie burzy cytokinowej dochodzi do gwałtownej aktywacji komórek układu odpornościowego. Szybkich podziałów limfocytów T i limfocytów B, monocytów, makrofagów, komórek dendrytycznych i komórek NK oraz nadprodukcji przez nie ponad 150 różnych cytokin.
Cechą burzy cytokinowej jest utrata możliwości przez układ odpornościowy negatywnego sprzężenia zwrotnego, które fizjologicznie zahamowuje nadmierną produkcję cytokin prozapalnych. Uwalnianie cytokin indukuje uwalnianie kolejnych cytokin, co z inicjuje reakcję łańcuchowa nie do zatrzymania. Dochodzi do rodzaju samonapędzającego się błędnego koła.
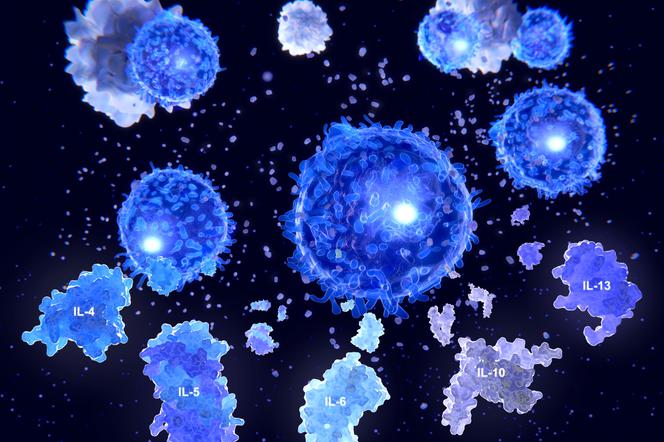
Cytokiny to zróżnicowana grupa niewielkich molekuł, które są głównie wydzielane przez komórki układu odpornościowego w celu wzajemnej komunikacji. Wśród najważniejszych funkcji jakie pełnią cytokiny to kontrola podziałów i różnicowania komórek odpornościowych oraz regulacja reakcji zapalnej.
Do cytokin należą takie białka jak:
- Interferony (IFN), które odgrywają główną rolę we wrodzonej odporności na wirusy i inne drobnoustrojowe
- Interleukiny (IL), które regulują przede wszystkim różnicowanie i aktywację komórek odpornościowych. Mogą pełnić funkcje prozapalne (aktywujące odpowiedź zapalna) lub przeciwzapalne (hamujące odpowiedź zapalną)
- Chemokiny działają jako substancje „przyciągające” komórki układu odpornościowego przez co kontrolują ich przemieszczanie do miejsc reakcji zapalnej
- Czynniki stymulujące tworzenie kolonii (CSF) kontrolują hematopoezę, czyli proces wytwarzanie dojrzałych komórek układu odpornościowego z macierzystych komórek krwi
- Czynnik martwicy nowotworów (TNF) jest prawdopodobnie najlepiej przebadaną cytokiną prozapalną, która odgrywa centralną rolę w burzy cytokinowej
Burza cytokinowa – przyczyny
Czynniki prowadzące do powstania burzy cytokinowej są związane z szeroką gamą chorób zakaźnych i niezakaźnych. Do czynników zakaźnych należą:
- paciorkowce z grupy A
- wirus cytomegalii
- wirus Epstein-Barr
- wirus Ebola
- wirus grypy
- wirus ospy
- koronawirusy np. SARS-CoV, MERS-CoV
Do czynników niezakaźnych należą:
- choroba przeszczep przeciwko gospodarzowi
- stwardnienie rozsiane
- młodzieńcze idiopatyczne zapalenie stawów
- zapalenie trzustki
- nowotwory np. chłoniaki
- terapie biologiczne np. rytuksymab
- zespół hemofagocytarny
- zespół aktywacji makrofagów
Jedną z największych zagadek związanych z burzą cytokinową jest to, dlaczego niektóre osoby wydają się być szczególnie podatne, a inne oporne na rozwiniecie się burzy cytokinowej. Prawdopodobnie jest to związane z genetyczną zmiennością odpowiedzi odpornościowej w populacji człowieka.
Burza cytokinowa – konsekwencje
Burza cytokinowa jest ważną przyczyną śmiertelności u pacjentów zakażonych wirusami, takimi jak Ebola, Marburg, koronawirusy, czy grypa pandemiczna. Częstą konsekwencją burzy cytokinowej w przypadku wirusów atakujących płuca np. SARS-CoV i wirusem grypy jest ostre uszkodzenie płuc (ALI, ang. acute lung injury).
ALI charakteryzuje się ostrą odpowiedzią zapalną tkanki płucnej, po której następuje przewlekła faza odkładania kolagenu w płucach i ich włóknienie. ALI może z czasem przekształcić się w jego cięższą postać, czyli zespół ostrej niewydolności oddechowej (ARDS, ang. acute respiratory distress syndrome).
Miejscowe zapalenie płuc może rozlać się poprzez układ krążenia na cały organizm, siejąc zniszczenie w postaci uszkodzenia innych narządów. Ostatecznie można zaobserwować ciężki zespół kliniczny pod postacią sepsy.
Osoby z ciężką sepsą spowodowaną zakażeniami wykazują charakterystyczne profile cytokin we krwi, które zmieniają się w czasie. Cytokiny ostrej odpowiedzi to TNF, interleukina-1 i 8, które pojawiają się we wczesnych minutach lub godzinach od zakażeniu, po czym następuje wyraźny wzrost poziomu interleukiny-6. Przeciwzapalna interleukina-10 pojawia się nieco później, gdy organizm próbuje kontrolować ostrą ogólnoustrojową odpowiedź zapalną.
Oprócz zakażeń płuc burza cytokinowa jest konsekwencją ciężkich zakażeń przewodu pokarmowego, dróg moczowych, ośrodkowego układu nerwowego, skóry oraz przestrzeni stawowych.
Burza cytokinowa – objawy
- gorączka
- zmęczenie
- utrata apetytu
- ból mięśni i stawów
- nudności i wymioty
- biegunka
- spadek ciśnienia krwi
- przyspieszone bicie serca
- drgawki
- ból głowy
- majaczenie i omamy
- splątanie
- wysypka
Natomiast w badaniach laboratoryjnych stwierdza się wysoki poziom:
- związków azotu we krwi
- D-dimerów
- aminotransferaz
- ferrytyny
- białka CRP
- interleukiny-6
- dehydrogenazy mleczanowej
- przedłużony czas protrombinowy
- zmniejszoną liczbę płytek krwi
Burza cytokinowa – leczenie
Obecnie nie ma jednej terapii burzy cytokinowej i leków przeznaczonych specjalnie do jej leczenia. Główne podejście w leczeniu tego zespołu to wywołanie immunosupresji, czyli zmniejszeniu reaktywności układu odpornościowego. W tym celu stosowane są takie leki jak:
- kortykosteroidy
- inhibitory cytokin np. tocilizumab
Burza cytokinowa – COVID-19 i inne pandemie
Zgromadzone dowody kliniczne sugerują, że podgrupa pacjentów z ciężkim przebiegiem COVID-19 wywołana zakażeniem wirusem SARS-CoV-2 może wykazywać zespół burzy cytokinowej.
Wieloośrodkowe retrospektywne badania opublikowane przez Ruan i wsp. w których przeanalizowano 150 potwierdzonych przypadków COVID-19 wykazały, że śmiertelność COVID-19 może wynikać z aktywowanej wirusem burzy cytokinowej. U tych chorych zaobserwowano podwyższone poziomy ferrytyny i interleukiny-6 we krwi. Może mieć to ważne implikacje w leczeniu choroby, gdyż aktualnie leczenie COVID-19 ma charakter wspomagający.
Dlatego sugeruje się, że u pacjentów z ciężkim przebiegiem COVID-19 powinno się wykonywać badania przesiewowe w kierunku burzy cytokinowej (np. poprzez oznaczenie poziomu ferrytyny) w celu zidentyfikowania podgrupy pacjentów, u których leczenie immunosupresyjne byłoby skuteczne. W Klinice Chorób Zakaźnych Samodzielnego Publicznego Szpitala Klinicznego nr 1 w Lublinie testuje się właśnie to nowe podejście terapeutyczne.
Burza cytokinowa może tłumaczyć śmiertelność wśród osób młodych na COVID-19, gdyż analogiczną sytuację zaobserwowano w 1918 roku podczas pandemii grypy hiszpanki. Wtedy ponad połowa zgonów miała miejsce u osób ogólnie zdrowych między 18. a 40. rokiem życia i była spowodowana właśnie burzą cytokinową, która doprowadziła do zespołu ostrej niewydolności oddechowej.
Z drugiej strony zjawisko burzy cytokinowej wyjaśnia, dlaczego dzieci łagodnieje przechodzą zakażenie wirusem SARS-CoV-2. Ich układ odpornościowy jest po prostu słabiej rozwinięty i nie reaguje tak gwałtownie na obecność wirusa.
Czytaj też:
- Jak przebiega zakażenie koronawirusem SARS CoV-2? Nowe ustalenia!
- Koronawirus niebezpieczny dla osób starszych - jak chronić seniorów?
- Dlaczego koronawirus zabija młodych?
- Lekarz pokazuje, jak koronawirus niszczy płuca młodych ludzi
- Śmiertelność u osób zarażonych koronawirusem