Spis treści
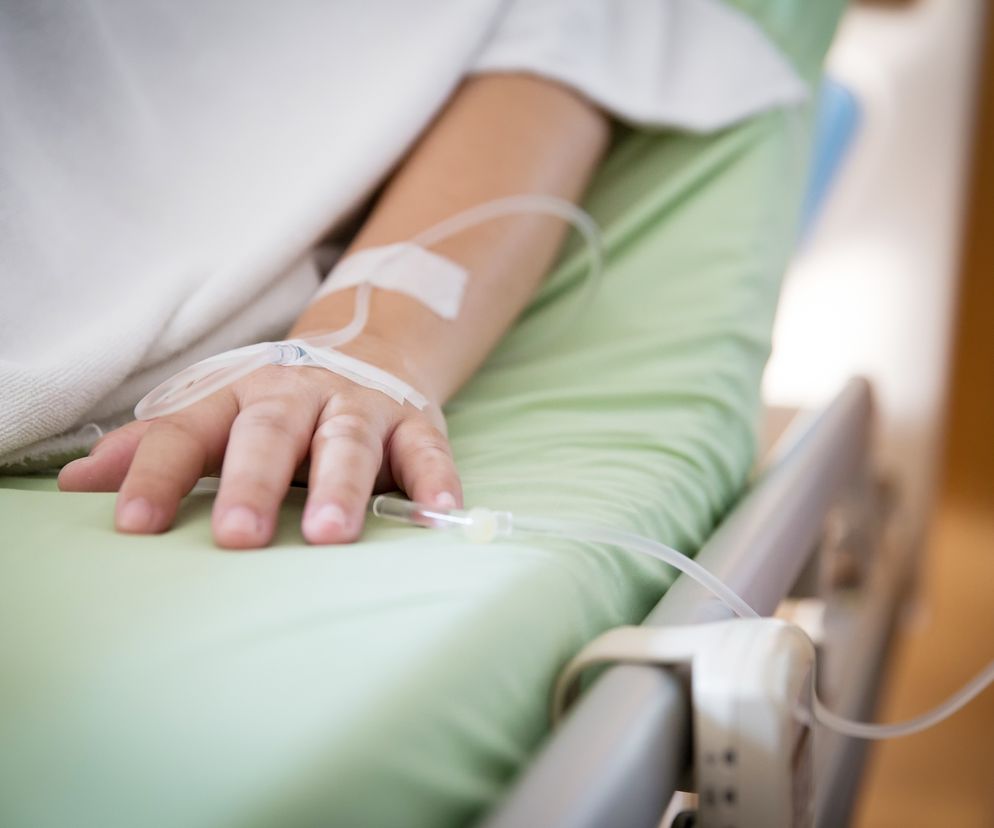
"Żółta chemia" jest jednym z określeń używanych przez lekarzy w odniesieniu do leczenia onkologicznego. W środowisku pacjentów onkologicznych oraz lekarzy onkologów, poza nazwami chemicznymi oraz żargonem specjalistycznym, operuje się czasami potocznymi nazwami nawiązującymi do koloru podawanych leków. Chemioterapia bardzo często aplikowana jest w postaci dożylnej – jako serii pojedynczych zastrzyków lub tzw. wlewu kroplowego, podawanego powoli nawet przez kilkanaście godzin. Mieszanina umieszczana w podajniku lub w strzykawce zawiera zwykle „koktajl” kilku cytostatyków, których uzupełniające się spektrum działania ma zapewnić jak najlepszy efekt eliminujący komórki rakowe.
Kolory chemioterapii
Wyróżnia się 3 główne kolory chemioterapii:
- Chemia czerwona – jedna z najbardziej agresywnych form terapii onkologicznych, stosowana najczęściej w formie wlewów m.in. przy białaczkach, raku pęcherza moczowego, raku prostaty. Jaskrawy, rubinowy kolor nadaje jej doksorubicyna – silny cytostatyk z rzędu antracyklin. Dodatkowo w roztworze mogą być obecne także inne leki, np. epirubicyna czy cyklofosfamid.
- Chemia biała – uważana za mniej szkodliwą od pozostałych form chemioterapii, jej głównym składnikiem jest bleomycyna, która po rozpuszczeniu daje bezbarwny, klarowny roztwór. Ten cytostatyk stosowany jest m.in. w terapii raka płaskonabłonkowego głowy i szyi, zewnętrznych narządów płciowych, raku szyjki macicy oraz raku jądra.
- Chemia żółta – wykorzystywana jako terapia uzupełniająca leczenia raka piersi i podawana w cyklach jako wlewy dożylne. Mieszanina zawiera najczęściej cyklofosfamid, 5-fluorouracyl oraz metotreksat (który nadaje roztworowi intensywną, żółtą barwę).
Oczywiście, nie znając dokładnego składu podawanego preparatu (a jedynie oceniając kolor wlewu), nie da się określić jego działania ani potencjalnych efektów ubocznych. Receptura i harmonogram terapii onkologicznych jest zawsze ustalany indywidualnie i konsultowany z najnowszymi zaleceniami i wytycznymi krajowymi.
Kiedy stosuje się żółtą chemię?
Chemioterapia „żółta” stosowana jest głównie w terapiach raka piersi. Obecnie jest to najczęściej występujący u kobiet nowotwór złośliwy, a ilość wykrytych przypadków w krajach europejskich z roku na rok rośnie. Niestety, rak ten (tuż po raku oskrzeli i raku płuca) związany jest z wysokim odsetkiem śmiertelności, co jest ogromnym problemem szczególnie w Polsce. Zaledwie w ciągu jednego roku na zaawansowanego raka piersi umiera blisko 10 000 kobiet w naszym kraju.
Znanych jest wiele czynników ryzyka, które mogą mieć wpływ na rozwój choroby, niektóre z nich to np.:
- wiek powyżej 35 r.ż
- czynniki genetyczne (mutacje genów: BRCA1, BRCA2, p53, ATM przekazywane np. z matki na córkę)
- czynniki hormonalne (przyjmowanie antykoncepcji hormonalnej lub hormonalnej terapii zastępczej w starszym wieku)
O tym, jakie leczenie zostanie włączone w konkretnym przypadku raka piersi, decydują specjaliści po wykonaniu dokładnych badań diagnostycznych.
Niezbędne jest zaklasyfikowanie wykrytej zmiany wg. kryteriów TNM (od ang. T- tumor (guz); N-nodus (węzeł); M-metastases (przerzuty)) – czyli skali oceniającej nie tylko wielkość samego guza, ale także stan lokalnych węzłów chłonnych i ewentualne występowanie przerzutów odległych.
Na podstawie biopsji pobieranej z guza określa się również typ histologiczny, obecność receptorów estrogenowych i progesteronowych oraz receptorów HER2. Wszystko to ma na celu określenie sygnałów, które potencjalnie stymulują komórki nowotworowe do wzrostu i zaplanowanie najbardziej skutecznej terapii.
Niestety, pomimo zaawansowania współczesnej medycyny, żaden czynnik rokowniczy ani diagnostyka nie jest w stanie w 100% przewidzieć przebiegu choroby u danej pacjentki.
Jeszcze do niedawna rutynowym leczeniem raków piersi było standardowe chirurgiczne polegające na usunięciu całej piersi. Obecnie jednak odchodzi się od tej radykalnej metody stosując tzw. operację oszczędzającą (szczególnie jeśli wielkość wykrytego guza wynosi poniżej 3 cm i nie stwierdzono przerzutów do węzłów chłonnych).
Aby zapewnić maksymalną skuteczność leczenia i pewność, że choroba nie powróci dodatkowo stosuje się chemioterapię – silnie działające leki hamujące namnażanie się komórek.
Tego typu terapia systemowa może być stosowana przed planowanym zabiegiem chirurgicznym (aby zmniejszyć masę guza) lub też po zabiegu – jako leczenie uzupełniające (tzw. leczenie adjuwantowe).
Choć niemal każda forma chemioterapii jest niezwykle szkodliwa dla organizmu, mało selektywna i powoduje zwykle szereg skutków ubocznych – w niektórych przypadkach raka piersi tego typu dodatkowe leczenie będzie wymagane. Taka potrzeba zaistnieje m.in. gdy:
- guz nowotworowy cechuje się bardzo szybkim wzrostem,
- pojawiły się przerzuty odległe,
- analiza histopatologiczna wykazała brak receptorów estrogenowych i progesteronowych.
Zwłaszcza ta ostatnia cecha jest złym prognostykiem dla skuteczności leczenia, ponieważ oznacza, że komórki rakowe są niewrażliwe na inne, bardziej wybiórcze rodzaje leczenia, np. hormonoterapię. Chemioterapia o szerokim spektrum działania (m.in. cytostatyki wchodzące w skład żółtej chemii) staje się wtedy leczeniem z wyboru.
Składniki żółtej chemii
Najczęściej stosowanymi lekami, wchodzącymi w skład żółtego wlewu są 3 popularne cytostatyki:
Metotreksat
Substancja ta została wprowadzona do leczenia już w latach 50. XX wieku, jednak nadal figuruje na liście leków podstawowych opublikowanej przez Światową Organizację Zdrowia (WHO).
Metotreksat jest tzw. antywitaminą (antagonistą) kwasu foliowego, co oznacza, że praktycznie nieodwracalnie zaburza wszelkie przemiany biochemiczne wszystkich pochodnych tego związku.
Z kolei kwas foliowy pełni w organizmie bardzo złożone funkcje - współuczestniczy w syntezie aminokwasów, zasad wykorzystywanych do syntezy DNA i RNA, jest też „nośnikiem” grup jednowęglowych w wielu reakcjach.
Metotreksat jest terapeutykiem o działaniu nie tylko przeciwnowotworowym (hamującym podziały komórkowe), ale też immunosupresyjnym (hamującym odpowiedź układu odpornościowego).
Wykorzystuje się go podczas walki z chorobami nowotworowymi:
- ostrych białaczkach (limfatycznej i szpikowej)
- raku sutka,
- raku jajnika,
- raku płuca,
- nowotworach litych głowy i szyi.
Metotreksat może być podawany nie tylko w postaci wlewu dożylnego, ale też niekiedy doustnie w formie tabletek. Lek jest wydalany w 90% wraz z moczem.
W dużo mniejszych dawkach metotreksat stosowany jest też w przebiegu chorób reumatoidalnych o podłożu autoimmunologicznym (np. reumatoidalnego zapalenia stawów RZS lub zesztywniającego zapalenia stawów kręgosłupa) jako tzw. lek modyfikujący przebieg choroby (LMPCh).
5-Fluorouracyl (5-FU)
5-Fluorouracyl (5-FU) jest organicznym związkiem chemicznym i fluorową pochodną uracylu - zasady budującej RNA. W wyniku jego działania, powstające RNA wykazuje nieprawidłową budowę i upośledzone funkcje, co skutkuje uszkodzeniem i śmiercią komórki. Cytostatyczny efekt fluorouracylu widoczny jest szczególnie w tkankach silnie zróżnicowanych i szybko rosnących (np. skóra, błony śluzowe, szpik kostny).
5-fluorouracyl najczęściej stosuje się w terapii:
- raka piersi,
- raka jelita grubego,
- raka żołądka,
- raka trzustki,
- nowotworach szyjki macicy,
- nowotworach jajnika.
Poza podaniem dożylnym, lek ten czasem bywa stosowany w postaci maści na rogowaciejące lub przedrakowe zmiany skórne, gdzie wspomaga ich gojenie.
Cyklofosfamid
Cyklofosfamid (znany też jako komercyjny preparat - Endoxan) – to jednej z najczęściej stosowanych cytostatyków, z powodzeniem wykorzystywany w terapiach przeciwnowotworowych. Ciekawostką jest fakt, że pod względem budowy chemicznej jest on pochodną iperytów azotowych – a więc związków zaliczanych do niebezpiecznych, parzących bojowych środków trujących.
Po podaniu do ustroju, ulega przekształceniu do aktywnych metabolitów dopiero w wątrobie. Związki te posiadają charakterystyczne właściwości alkilujące, polegające na przenoszeniu grup chemicznych w cząsteczkach funkcjonalnych związków.
Takie modyfikacje budowy powodują trwałe uszkodzenia białek, łańcuchów DNA i RNA, hamując tym samym prawidłowe podziały komórkowe (zwłaszcza w tkankach szybko dzielących się).
Cyklofosfamid stosowany jest m.in. w terapiach :
- raka sutka,
- ostrych białaczek,
- szpiczaka mnogiego,
- ziarnicy złośliwej,
- drobnokomórkowego raka płuc,
- raka trzonu macicy.
Związek ten może być też czasami wykorzystywany w leczeniu ciężkich postaci schorzeń tkanki łącznej (kolagenoz) o podłożu autoimmunologicznym, jak:
- reumatoidalne zapalenie stawów (RZS),
- toczeń rumieniowaty układowy,
- twardzina układowa,
- Zespół Sjögrena.
Podobnie jak metotreksat, cyklofosfamid można podawać zarówno doustnie (w tabletkach), jak i dożylnie w postaci wlewu kroplowego.
Potencjalne skutki uboczne żółtej chemii
Połączenie działania 3 silnych cytostatyków w jednym preparacie „żółtej chemii” bez zwątpienia zwiększa szanse wyeliminowania z organizmu komórek nowotworowych. Niestety, przekłada się to też na większe ryzyko występowania uciążliwych dla pacjentów działań niepożądanych. Nie u wszystkich leczonych wystąpią podobne skutki uboczne. Reakcja na leczenie zależy od bardzo wielu czynników, m.in.:
- wieku,
- wyniszczenia organizmu,
- chorób współistniejących,
- innych przyjmowanych leków.
Ponieważ wszystkie 3 wymienione składniki „żółtej chemii” wykazują szerokie działanie ogólnoustrojowe, niezwykle ciężko będzie ustalić, który cytostatyk wywołał dany objaw niepożądany. Niektóre jednak symptomy pojawiają się u pacjentów statystycznie częściej niż inne. Na jakie skutki uboczne powinien przygotować się pacjent przyjmujący „żółtą chemię”?
- Obniżona odporność na infekcje – zarówno metotreksat, jak cyklofosfamid i 5-fluorouracyl mogą trwale uszkadzać szpik kostny, odpowiedzialny za wytwarzanie białych krwinek układu immunologicznego (tzw. neutropenia). To z kolei przełoży się na zwiększoną podatność na typowe przeziębienia, ale też choroby grzybicze lub bakteryjne. Aby nie dopuścić do zbytniego spadku liczby białych krwinek, przed każdym kolejnym cyklem chemioterapii wykonywane są badania krwi.
- Chroniczne zmęczenie i osłabienie – działanie stosowanych cytostatyków jest nieselektywne, co oznacza, że uszkadzają one komórki zarówno nowotworowe jak i zdrowe. Organizm osoby poddawanej terapii toczy więc ciężką walkę, co w miarę kolejnych cykli przekłada się na jego wyniszczanie i uczucie osłabienia. Pacjenci powinni więc szczególnie dbać o odżywczą dietę i wypoczynek, a także unikać prowadzenia samochodu lub obsługi skomplikowanych maszyn.
- Wymioty, biegunki i objawy gastryczne – objawy ze strony przewodu pokarmowego występują dość często przy stosowaniu cyklofosfamidu i metotreksatu. Wynika to silnego działania tych substancji na nabłonek przewodu pokarmowego, które często powoduje nawet stany zapalne błon śluzowych. Dojmujące objawy czasami wymagają dodatkowego wspomagania lekami przeciwwymiotnymi i przeciwbiegunkowymi. Aby nie dopuścić do odwodnienia, pacjentom zaleca się picie dużej ilości napojów.
- Wypadanie włosów i łysienie - choć jest jednym z objawów o najmniej istotnym wpływie dla globalnego zdrowia organizmu, wiele osób odbiera go jako najbardziej dotkliwy ze względów estetycznych. Symptom ten jest charakterystyczny dla działania wszystkich 3 składowych „żółtej chemii”. Przerzedzanie włosów rozpoczyna się zwykle już po 3-4 tygodniach od rozpoczęcia leczenia, a stopniowo może obejmować też wypadanie brwi i rzęs lub owłosienia ciała. Na szczęście po zakończonej terapii włosy odrastają – choć czasami mogą przyjmować inny odcień lub strukturę niż wcześniej.
Wymienione symptomy to tylko niektóre z nieprzyjemnych dolegliwości jakie mogą wystąpić po cyklu terapii onkologicznej. Aby wygrać walkę z nowotworem warto jednak stawić im czoła.
Polecany artykuł: