Choroby genetyczne
Choroby genetyczne są szeroką grupą patologii, które są spowodowane mutacjami w obrębie jednego lub kilku genów. Wbrew pozorom, nie wszystkie choroby o podłożu genetycznym mogą być dziedziczone. Jeśli mutacja DNA zajdzie jedynie w komórkach somatycznych (czyli zróżnicowanych komórkach tworzących wszystkie organy) – taka „wada” nie będzie przenoszona na potomstwo. Natomiast choroby wywołane przez mutacje w komórkach rozrodczych (plemnikach i komórkach jajowych) będą dziedziczone.
Rodzaj chorób genetycznych jest ściśle związany z tym, jak rozległe zmiany zaszły w materiale genetycznym. Do rozwoju niektórych schorzeń wystarczy pojedyncza, specyficzna mutacja punktowa, podczas gdy inne objawiają się dopiero przy zaburzeniach funkcjonowania całych chromosomów lub grup genów, powstających na przykład podczas błędów podziałów komórkowych.
Dziedziczenie chorób jednogenowych zachodzi ściśle według praw opracowanych przez Mendla. W zależności od tego czy choroba ujawnia się już przy zaistnieniu jednej wersji błędnego genu w parze alleli czy obu, wyróżnia się wersje dziedziczenia: autosomalne recesywne lub autosomalne dominujące. Ważną grupą chorób genetycznych są schorzenia sprzężone z płcią – czyli ściśle związane z tym, czy mutacja genowa występuje na chromosomie X. Przy obu wersjach chromosomu X (u kobiet) nie dochodzi do rozwoju oznak choroby, chorują natomiast osobniki płci męskiej z jedną wersją chromosomu X i jednym Y. Choroby sprzężone z płcią to np. hemofilia, daltonizm czy dystrofia mięśniowa Duschenn’a.
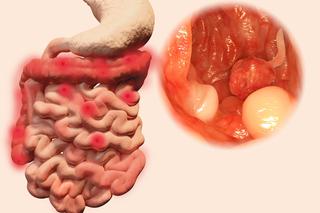
Objawy chorób genetycznych mogą być skrajnie różnorodne: od niezauważalnych gołym okiem zaburzeń metabolicznych, aż po ciężkie upośledzenie rozwoju i wady anatomiczne. Niektóre poważne zespoły zaburzeń genetycznych okazują się śmiertelne już w życiu płodowym, w innych przypadkach chorzy są w stanie żyć komfortowo przez kilkadziesiąt lat. Patologie genetyczne diagnozowane są znacznie rzadziej od chorób warunkowanych np. stylem życia, jednak ich leczenie stanowi zwykle duże wyzwanie dla medycyny. Terapie polegają najczęściej łagodzeniu objawów choroby lub fizjoterapii.
![Dziedziczenie trombofilii [Porada eksperta]](https://cdn.galleries.smcloud.net/t/galleries/gf-NFUB-jCnw-iT7X_porada-genetyka-320x213.jpg)