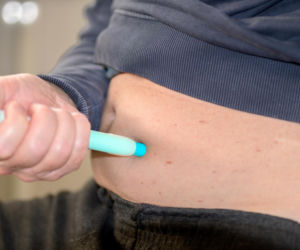
Nowotwory krwi mogą dawać różne objawy
Nowotwory krwi, zwane również nowotworami hematologicznymi, często zaczynają się w szpiku kostnym, gdzie powstają i dojrzewają komórki krwi. W ciągu naszego życia w komórkach krwiotwórczych gromadzą się mutacje DNA, co prowadzi do powstawania nowotworów. Nowotwory krwi mogą dawać różne objawy, które często są niespecyficzne i dlatego łatwo je przeoczyć.
W momencie, gdy komórki nowotworowe zaczynają się dzielić w niekontrolowany sposób, normalne komórki krwi nie są wytwarzane w wystarczającej ilości. Dochodzi do sytuacji, w której zdrowe komórki nie są w stanie prawidłowo funkcjonować, np. zwalczać infekcji.
Wśród różnorodnych nowotworów hematologicznych możemy wyróżnić białaczki, chłoniaki czy szpiczaka mnogiego. Dodatkowo istnieje wiele innych chorób układu krwiotwórczego, z których część może się przekształcić w nowotwór. Do najczęściej występujących zaliczamy niedokrwistość, zaburzenia krzepnięcia i zespoły mielodysplastyczne (MDS).
Na czym polega mobilizacja komórek krwi?
W sytuacji stresowej dla organizmu, np. podczas infekcji lub utraty krwi, proces produkcji komórek krwi ulega przyspieszeniu i ich duża ilość, w tym także komórki macierzyste i niedojrzałe komórki krwi, są uwalniane ze szpiku kostnego do krwi obwodowej. Ten proces nazywa się mobilizacją. W mobilizację komórek zaangażowany jest czynnik wzrostu kolonii granulocytów, czyli G-CSF. Białko to można wyprodukować w bakteriach i użyć jako leku.
Regulacja mobilizacji komórek krwi ze szpiku kostnego do krwiobiegu jest więc procesem, w który można ingerować farmakologicznie. Farmakologiczna indukcja mobilizacji jest szczególnie istotna przy przeszczepianiu krwiotwórczych komórek macierzystych, ponieważ daje możliwość ich izolacji z krwi obwodowej dawcy, zamiast ze szpiku kostnego.
Mobilizacja komórek odgrywa także istotne znaczenie w przypadku chorych na inne nowotwory. U pacjentów poddanych chemioterapii często dochodzi do obniżenia liczby komórek krwi, co zwiększa ryzyko infekcji, a w konsekwencji może skutkować koniecznością przerwania leczenia. W takich przypadkach chorzy otrzymują białko G-CSF, które mobilizuje komórki pochodzące ze szpiku kostnego do krwiobiegu.
Polka poszukuje nowych metod leczenia
Niestety, mobilizacja przy pomocy G-CSF nie u każdego pacjenta przynosi spodziewane efekty. Co więcej, sam proces wytworzenia białka jest kosztowny i skomplikowany. Dlatego naukowcy ciągle poszukują nowych metod terapeutycznych.
Jedną z takich osób jest dr Agata Szade, stypendystka 21. edycji programu L’Oréal-UNESCO Dla Kobiet i Nauki. Podczas studiów doktoranckich odkryła, że protoporfiryna kobaltu wywołuje produkcję białka G-CSF w organizmie, a tym samym powoduje mobilizację komórek szpiku kostnego do krwi.
Dr Szade podkreśla: "Obecnie trwają badania przedkliniczne na gryzoniach. Przede wszystkim chcemy potwierdzić, że protoporfiryna kobaltu działa tak efektywnie, jak możemy wnioskować z naszych badań wstępnych, ale również, czy nasza metoda nie daje poważnych skutków ubocznych. Jeśli okaże się skuteczna i bezpieczna, jest szansa, że w przyszłości będzie dodatkową możliwością terapii".
Komu pomoże nowa terapia?
Badania dr Agaty Szade mogą być szansą na lepsze leczenie wielu pacjentów. Ekspertka wyjaśnia: "Badania nad nowymi mechanizmami mobilizacji mają duże znaczenie w przypadku pacjentów chorych na nowotwory krwi. Jeśli nasze założenia się potwierdzą, to protoporfiryna kobaltu ma duży potencjał aplikacyjny. Oprócz leczenia skutków ubocznych chemioterapii, mogłaby być przydatna w przeszczepieniach krwi mobilizowanej".
- To daje nadzieję na stworzenie nowych metod leczniczych, które będą wspierać walkę wielu chorych z nowotworami krwi – dodaje dr Agata Szade.

Dr Agata Szade ukończyła studia na kierunku biotechnologia na Wydziale Biochemii, Biofizyki i Biotechnologii Uniwersytetu Jagiellońskiego. W 2010 roku ukończyła podwójne Francusko-Polskie studia magisterskie, broniąc pracy dotyczącej roli interleukiny-1 w zapaleniu płuc wywołanym Pseudomonas aeruginosa. Następnie rozpoczęła studia doktoranckie na WBBiB UJ, badając rolę oksygenazy hemowej-1 w raku płaskonabłonkowym. Podczas tych badań zaobserwowała nieznane wcześniej działanie protoporfiryny kobaltu, wywołujące mobilizację komórek szpiku kostnego do krwi.
Po obronie doktoratu, dzięki grantowi Mobilność Plus MNiSW, wyjechała na 2-letni staż podoktorski do laboratorium dr Eugene’a Butchera na Uniwersytecie Stanforda. Za pracę naukową podczas studiów magisterskich i doktorskich otrzymała m.in. Stypendium Ministra Nauki i Szkolnictwa Wyższego za osiągnięcia w nauce, Stypendium Małopolskiej Fundacji Stypendialnej Sapere Auso za szczególne osiągnięcia naukowe, Stypendium „Doctus - Małopolski fundusz stypendialny dla doktorantów” oraz zajęła drugie miejsce w konkursie "Dziewczyny Przyszłości. Śladami Marii Skłodowskiej-Curie" organizowanym przez Ministerstwo Nauki i Szkolnictwa Wyższego oraz miesięcznik Elle.
Jest także laureatką Stypendium Ministra Nauki i Szkolnictwa Wyższego dla wybitnych młodych naukowców. Dzięki grantom Fundacji DKMS, Narodowego Centrum Nauki (Sonata) oraz Narodowego Centrum Badań i Rozwoju (Lider) kontynuuje badania nad mobilizacją komórek szpiku kostnego