Nowy przegląd opublikowany w „British Journal of Clinical Pharmacology” analizuje, jak bakterie jelitowe wpływają na skuteczność semaglutydu, liraglutydu i dulaglutydu oraz czy możliwa jest personalizacja terapii.
Mikrobiom jelitowy a leki GLP-1
Ponad 500 milionów osób na świecie żyje z cukrzycą typu 2, a wskaźniki otyłości nadal rosną. Agoniści receptora glukagonopodobnego peptydu 1, czyli GLP-1RAs, zmieniły standard leczenia, poprawiając kontrolę glikemii, wspierając redukcję masy ciała oraz zmniejszając ryzyko sercowo-naczyniowe. Wciąż jednak nie ma jednoznacznej odpowiedzi, dlaczego część pacjentów reaguje na terapię znacznie lepiej niż inni. W przeglądzie dotyczącym GLP-1 opublikowanym w 2026 roku w British Journal of Clinical Pharmacology autorzy Kamath S, Chan NSL i Joyce P analizują relacje między agonistami GLP-1 a mikrobiomem jelitowym. Zwracają uwagę, że bakterie jelitowe wpływają na metabolizm, funkcjonowanie układu odpornościowego oraz sygnalizację hormonalną, a ich skład może modulować zarówno endogenne wydzielanie GLP-1, jak i odpowiedź terapeutyczną na leki.
Jak bakterie jelitowe regulują hormony?
GLP-1 jest hormonem wydzielanym przez komórki enteroendokrynne typu L w jelicie. Stymuluje wydzielanie insuliny, obniża poziom glukagonu, spowalnia opróżnianie żołądka i zwiększa uczucie sytości. Procesy te mają bezpośrednie znaczenie dla kontroli glikemii i masy ciała. Bakterie jelitowe rozkładają błonnik pokarmowy do krótkołańcuchowych kwasów tłuszczowych, takich jak octan, propionian i maślan. Te metabolity aktywują receptory sprzężone z białkiem G, w tym GPR41 i GPR43, co może stymulować wydzielanie GLP-1 poprzez mechanizmy obejmujące modulację wapnia wewnątrzkomórkowego i przekaźnika cAMP. Maślan może dodatkowo hamować deacetylazę histonową, zwiększając transkrypcję genu proglukagonu.
Kwasy żółciowe także uczestniczą w regulacji. Pierwotne kwasy żółciowe, takie jak kwas cholowy i chenodeoksycholowy, przekształcane są przez bakterie jelitowe w formy wtórne, które aktywują receptor TGR5 i nasilają wydzielanie GLP-1. Z kolei aktywacja receptora FXR może hamować jego syntezę. W przypadku dysbiozy zwiększone stężenie lipopolisacharydu aktywuje receptor TLR4 oraz szlak NF-κB, prowadząc do produkcji cytokin zapalnych, w tym TNF-α i IL-6. Stan zapalny może osłabiać sygnalizację insuliny i wpływać na skuteczność terapii GLP-1.
GLP-1 a bakterie jelitowe w cukrzycy typu 2. Wpływ semaglutydu i liraglutydu
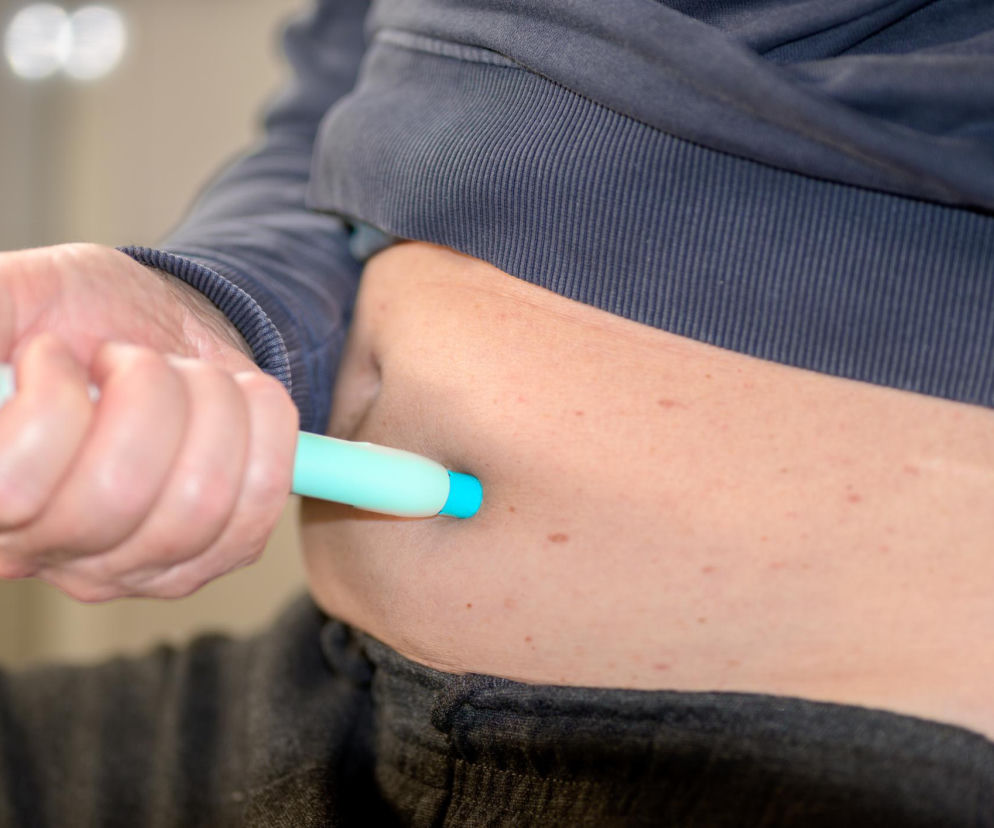
Leki z grupy GLP-1RAs, takie jak liraglutyd, semaglutyd i dulaglutyd, oddziałują nie tylko na gospodarkę węglowodanową, lecz także na apetyt, motorykę jelit oraz krążenie kwasów żółciowych, co może zmieniać skład mikrobiomu. W badaniach klinicznych i przedklinicznych obserwowano wzrost liczebności Akkermansia muciniphila oraz zmiany w proporcji Bacteroidetes do Firmicutes. U pacjentów z cukrzycą typu 2 liraglutyd wiązano z obniżeniem HbA1c, niewielką redukcją masy ciała i indeksu masy ciała oraz wzrostem Akkermansia muciniphila. W modelach zwierzęcych dieta wysokotłuszczowa połączona z podawaniem semaglutydu była związana ze spadkiem stosunku Firmicutes do Bacteroidetes, niższym stężeniem cytokin zapalnych i poprawą tolerancji glukozy.
Autorzy podkreślają, że zmiany mikrobiomu mogą wynikać nie tylko z bezpośredniego działania leków, lecz także z redukcji spożycia kalorii i utraty masy ciała. Dodatkowo leki takie jak metformina również modyfikują skład bakterii jelitowych, co utrudnia jednoznaczną interpretację danych i wskazuje na potrzebę kontrolowanych badań z monitorowaniem diety oraz analizą metabolomiczną.
Mikrobiom jelitowy a skuteczność leków GLP-1 w cukrzycy typu 2
Zmienność odpowiedzi na agonistów receptora GLP-1 pozostaje wyzwaniem klinicznym. W pilotażowym badaniu obejmującym 52 osoby z cukrzycą typu 2 stwierdzono, że pacjenci odpowiadający na terapię mieli odmienny wyjściowy profil mikrobiologiczny niż osoby bez poprawy. Gatunki takie jak Bacteroides dorei oraz Roseburia inulinivorans były powiązane z większym spadkiem HbA1c. W eksperymentach z przeszczepem mikrobioty kałowej przeniesienie bakterii od zwierząt leczonych do biorców poddanych antybiotykoterapii odtwarzało poprawę masy ciała i wrażliwości na insulinę, co sugeruje funkcjonalne znaczenie zmian mikrobiologicznych. Dane przyczynowe u ludzi pozostają jednak ograniczone.
Autorzy przeglądu podsumowują, że interakcja między GLP-1RAs a mikrobiomem jelitowym przebiega poprzez szlaki metaboliczne i zapalne. Metabolity bakteryjne regulują wydzielanie GLP-1, a same leki mogą modyfikować skład mikrobioty i potencjalnie wzmacniać efekty metaboliczne. Wskazują na potrzebę badań z kontrolą parametrów dietetycznych i długoterminową obserwacją, aby lepiej zdefiniować relacje między gospodarzem, mikrobiomem i lekiem w leczeniu otyłości oraz cukrzycy typu 2.
Dla pacjentów przyjmujących leki GLP-1, zrozumienie roli mikrobiomu jelitowego może otworzyć nowe perspektywy w optymalizacji terapii. Oprócz przestrzegania zaleceń lekarza, warto zwrócić uwagę na dietę bogatą w błonnik prebiotyczny, który wspiera rozwój korzystnych bakterii jelitowych. Konsultacja z dietetykiem w celu indywidualnego dopasowania planu żywieniowego, uwzględniającego skład mikrobiomu, może dodatkowo wzmocnić efekty leczenia i poprawić ogólny stan zdrowia.