Cilest ULOTKA
producent: Janssen-Cilag International N.V.
tabletki
Substancje czynne: Ethinylestradiol, Norgestimate
Kod ATC: G 03 A A 11
Synonimy:
Ethinylestradiol Aethinyloestradiolum; Ethinyl Estradiol; Éthinylestradiol; Ethinylestradiolum; Ethinyloestradiol; Etinilestradiol; Etinilestradiolis; Etinilöstradiol; Etinilösztradiol; Etinylestradiol; Etinyyliestradioli; Etynyloestradiol Norgestimate Dexnorgestrel Acetime; Norgestimaatti; Norgestimat; Norgestimato; Norgestimatum
Wskazania: antykoncepcja
UWAGA! Ulotka informacyjna dla pacjenta dołączona jest do opakowania leku. Zawiera informacje przeznaczone dla pacjenta na temat właściwego stosowania leku.
Cilest®
tabletki
Skład
Jedna tabletka zawiera:
0,250 mg Norgestimatum
0,035 mg Ethinyloestradiolum
Substancje pomocnicze:
Laktoza bezwodna, skrobia zmodyfikowana, magnezu stearynian, indygotyna – lak.
Opis działania
Preparat Cilest® hamuje wydzielanie gonadotropin w następstwie działania estrogenowego i progestagenowego etinyloestradiolu i norgestimatu. Podstawowym mechanizmem działania jest zahamowanie jajeczkowania. Do działania antykoncepcyjnego może przyczyniać się także zmiana właściwości śluzu szyjkowego oraz błony śluzowej trzonu macicy.
Inne działania nie związane z zapobieganiem ciąży.
Wpływ na miesiączki: zwiększenie regularności cyklu miesiączkowego, zmniejszenie utraty krwi i zmniejszenie zapadalności na niedokrwistość z niedoboru żelaza, zmniejszenie zapadalności na bolesne miesiączkowanie.
Działanie związane z hamowaniem owulacji: zmniejszenie zapadalności na czynnościowe torbiele jajnika, zmniejszenie częstości występowania ciąż ektopowych.
Inne działania: zmniejszenie zapadalności na włókniakogruczolaki, mastopatię, zmniejszenie zapadalności na ostre zapalne choroby miednicy, zmniejszenie zapadalności na raka endometrium, zmniejszenie zapadalności na raka jajnika.
Wskazania
Doustna antykoncepcja.
Przeciwwskazania
- Zakrzepowe zapalenie żył lub inne zaburzenia zakrzepowo-zatorowe
- Przebyte zakrzepowe zapalenie żył głębokich lub inne zaburzenia zakrzepowo-zatorowe
- Zaburzenia krążenia mózgowego lub choroba wieńcowa
- Migrena z aurą ogniskową
- Rozpoznany rak piersi lub podejrzenie o raka piersi
- Zastawkowa choroba serca z powikłaniami
- Ciężkie nadciśnienie (stałe skurczowe ciśnienie tętnicze równe lub powyżej 160 mm Hg a rozkurczowe równe lub powyżej 100 mm Hg)
- Cukrzyca z powikłaniami naczyniowymi
- Rak błony śluzowej trzonu macicy lub inny rozpoznany nowotwór zależny od estrogenów albo podejrzenie o taki nowotwór
- Niezdiagnozowane nieprawidłowe krwawienie z dróg rodnych
- Żółtaczka w następstwie zastoju żółci (cholestatyczna) w ciąży lub żółtaczka podczas stosowania doustnego preparatu antykoncepcyjnego w wywiadzie
- Ostra lub przewlekła choroba dotycząca komórek wątrobowych z zaburzeniami czynności wątroby
- Gruczolak lub rak wątroby
- Ciąża lub przypuszczenie ciąży
- Opryszczka ciężarnych w wywiadzie (rozpoznanie potwierdzone biopsją skóry)
- Nadwrażliwość na którykolwiek składnik preparatu
Ostrzeżenia specjalne i zalecane środki ostrożności
Określając stosunek ryzyka do korzyści ze stosowania doustnych preparatów antykoncepcyjnych należy sprawdzić, czy nie występują wymienione poniżej zaburzenia, które mogą zwiększać ryzyko powikłań związanych ze stosowaniem doustnej antykoncepcji:
- Zaburzenia, które mogą zwiększać ryzyko rozwoju żylnych powikłań zakrzepowo-zatorowych, np. długotrwałe unieruchomienie lub poważne zabiegi operacyjne
- Czynniki ryzyka chorób tętnic, np. palenie tytoniu, podwyższone stężenie lipidów w surowicy krwi (hiperlipidemia), nadciśnienie lub otyłość
- Nadciśnienie (stałe wartości skurczowego ciśnienia tętniczego w przedziale od 140 do 159 mm Hg, a rozkurczowego w przedziale od 90 do 99 mm Hg)
- Cukrzyca
- Ciężka depresja lub występowanie ciężkiej depresji w przeszłości
- Palenie tytoniu
Ogólne
Doustne preparaty antykoncepcyjne NIE CHRONIĄ przed zakażeniem wirusem nabytego niedoboru odporności (HIV) ani przed innymi chorobami przenoszonymi drogą płciową.
Przed przepisaniem doustnego preparatu antykoncepcyjnego należy przeprowadzić pełny wywiad i badanie fizykalne. Badania lekarskie należy powtarzać okresowo, zgodnie z ogólnie obowiązującymi zasadami.
Zaleca się sprawdzenie, jakie leki przyjmuje kobieta, która zgłosiła się w celu przepisania doustnego preparatu antykoncepcyjnego. Dotyczy to także preparatów ziołowych (szczególnie dziurawca zwyczajnego Hypericum perforatum). Należy zapoznać się z ulotkami dla pacjenta dołączonymi do leków przyjmowanych łącznie z doustnym preparatem antykoncepcyjnym (patrz Oddziaływanie z innymi lekami).
W przypadku występowania niezdiagnozowanego, utrzymującego się lub nawracającego krwawienia z dróg rodnych należy przeprowadzić odpowiednie badania, by wykluczyć obecność nowotworu złośliwego.
Doustny preparat antykoncepcyjny można zastosować nie wcześniej niż po trzech miesiącach od powrotu parametrów czynnościowych wątroby do wartości prawidłowych po przebytym zapaleniu wątroby. W przypadku ciężkiego zapalenia wątroby okres ten wynosić musi nie mniej niż sześć miesięcy.
Zaburzenia zakrzepowo-zatorowe i inne zaburzenia naczyniowe
Istnieją dowody na zwiększenie ryzyka występowania zaburzeń zakrzepowo-zatorowych i zaburzeń zakrzepowych w związku z przyjmowaniem doustnych preparatów antykoncepcyjnych. Względne ryzyko wśród kobiet przyjmujących doustne preparaty antykoncepcyjne jest większe w porównaniu do względnego ryzyka wśród kobiet nie przyjmujących takich preparatów odpowiednio: 3 razy w odniesieniu do częstości występowania po raz pierwszy zakrzepicy żył powierzchownych, 4 do 11 razy w odniesieniu do częstości występowania zakrzepicy żył głębokich lub zatorowości płucnej oraz 1,5 do 6 razy wśród kobiet z czynnikami predysponującymi do rozwoju żylnych zaburzeń zakrzepowo-zatorowych. Ryzyko rozwoju zaburzeń zakrzepowo-zatorowych związane z przyjmowaniem doustnych preparatów antykoncepcyjnych nie zależy od czasu trwania ich stosowania i zanika po zakończeniu przyjmowania preparatów.
U kobiet przyjmujących doustne preparaty antykoncepcyjne stwierdzono 2 do 4 krotne zwiększenie względnego ryzyka wystąpienia powikłań zakrzepowo-zatorowych po zabiegach operacyjnych. Ryzyko względne wystąpienia zakrzepicy żylnej jest dwa razy większe u kobiet z czynnikami usposabiającymi do ich rozwoju w porównaniu do kobiet bez takich czynników.
Gdy jest to możliwe w przypadku planowych zabiegów operacyjnych, które związane są z ryzykiem wystąpienia zaburzeń zakrzepowo-zatorowych stosowanie doustnych preparatów antykoncepcyjnych należy przerwać na co najmniej cztery tygodnie przed i dwa tygodnie po zabiegu, a także podczas przedłużającego się po zabiegu okresu nieruchomienia. Ponadto w okresie bezpośrednio po porodzie występuje zwiększone ryzyko rozwoju zaburzeń zakrzepowo-zatorowych, dlatego u kobiet nie planujących karmienia piersią doustne preparaty antykoncepcyjne należy przyjmować nie wcześniej niż po 3 tygodniach od dnia porodu. Po poronieniu, które nastąpiło w 20 tygodniu ciąży lub później doustne preparaty antykoncepcyjne można zastosować po 21 dniach od poronienia lub w pierwszym dniu pierwszego samoistnego krwawienia miesiączkowego, w zależności od tego co nastąpi wcześniej.
Względne ryzyko wystąpienia zakrzepicy tętnic (np. udar mózgu, zawał mięśnia sercowego) jest większe w obecności takich czynników usposabiających jak palenie papierosów, nadciśnienie tętnicze, podwyższone stężenie lipidów w surowicy krwi (hiperlipidemia), otyłość, cukrzyca, stan przedrzucawkowy w wywiadzie i starszy wiek. Wymienione poważne powikłania ze strony naczyń, występowały przy stosowaniu doustnych preparatów antykoncepcyjnych zawierających 50 mikrogramów lub więcej estrogenu. Ryzyko zaburzeń naczyniowych może być mniejsze w przypadku doustnych preparatów antykoncepcyjnych zawierających mniejsze dawki estrogenów i progestagenów.
Ryzyko wystąpienia poważnych działań niepożądanych ze strony układu sercowo-naczyniowego zwiększa się z wiekiem i przy paleniu dużej liczby papierosów. Ryzyko jest znaczne u kobiet w wieku powyżej 35 lat, które palą papierosy. Kobietom przyjmującym doustne preparaty antykoncepcyjne należy zalecać zaprzestanie palenia.
U kobiet przyjmujących doustne preparaty antykoncepcyjne opisywano przypadki wzrostu ciśnienia tętniczego krwi. Podwyższenie ciśnienia tętniczego krwi występuje częściej u starszych kobiet oraz u kobiet stosujących antykoncepcję przez długi okres. U wielu kobiet po zakończeniu przyjmowania doustnych preparatów antykoncepcyjnych nastąpił powrót ciśnienia tętniczego do wartości prawidłowych. Nie stwierdzono różnicy pod względem częstości występowania nadciśnienia tętniczego pomiędzy grupą kobiet, które kiedykolwiek w przeszłości przyjmowały doustne preparaty antykoncepcyjne a grupą kobiet, które tych preparatów nie przyjmowały nigdy.
U kobiet z nadciśnieniem tętniczym (utrzymujące się wartości w przedziale: ciśnienie skurczowe od 140 do 159 mm Hg / ciśnienie rozkurczowe od 90 do 99 mm Hg) przed rozpoczęciem stosowania doustnych preparatów antykoncepcyjnych należy obniżyć do wartości prawidłowych i kontrolować ciśnienie tętnicze. W razie znacznego podwyższenia ciśnienia tętniczego należy przerwać przyjmowanie doustnych preparatów antykoncepcyjnych.
Opisywano przypadki wystąpienia zakrzepicy siatkówki podczas przyjmowania doustnych preparatów antykoncepcyjnych. W razie niewyjaśnionej przemijającej, częściowej lub całkowitej utraty widzenia, wystąpienia zamazanego widzenia lub podwójnego widzenia, obrzęku plamki żółtej lub zmian naczyniowych siatkówki należy przerwać stosowanie doustnych preparatów antykoncepcyjnych. W sytuacjach takich należy natychmiast zdiagnozować przyczynę zaburzeń i zastosować odpowiednie leczenie.
Nowotwory wątroby
Zachorowalność na łagodne i złośliwe guzy wątroby, (gruczolaki wątroby i raki wątrobowokomórkowe) jest mała. Ryzyko wystąpienia tych guzów może zwiększać się w związku z faktem i długością okresu stosowania doustnych preparatów antykoncepcyjnych. Pęknięcie gruczolaków wątroby może być przyczyną zgonu ze względu na krwotok do jamy brzusznej.
Rak narządów rozrodczych i piersi
U kobiet, które obecnie przyjmują doustne preparaty antykoncepcyjne lub przyjmowały je w okresie ostatnich 10 lat występuje nieco większe ryzyko rozpoznania raka piersi, jednakże w przypadku rozpoznania raka zwykle jest on ograniczony do gruczołu piersiowego. Wiek, w którym kobieta kończy przyjmowanie doustnych preparatów antykoncepcyjnych jest ważnym czynnikiem ryzyka rozwoju raka piersi. Im późniejszy wiek zakończenia przyjmowania doustnych preparatów antykoncepcyjnych tym większe prawdopodobieństwo rozpoznania raka piersi. Czas trwania przyjmowania doustnych preparatów antykoncepcyjnych miał pod tym względem mniejsze znaczenie.
Kobieta powinna rozważyć możliwość zwiększenia ryzyka rozwoju raka piersi w stosunku do korzyści ze stosowania doustnych preparatów antykoncepcyjnych.
Wpływ na metabolizm
Doustne preparaty antykoncepcyjne mogą powodować zaburzenia tolerancji glukozy. Działanie takie jest bezpośrednio związane z dawką estrogenu. Żeńskie hormony płciowe o budowie sterydowej wytwarzane i wydzielane przez ciałko żółte jajnika w fazie lutealnej (progestageny) mogą zwiększać wydzielanie insuliny i powodować oporność tkanek na działanie insuliny, której nasilenie zależy od rodzaju stosowanego progestagenu. U kobiet zdrowych (bez cukrzycy) doustne preparaty antykoncepcyjne nie mają wpływu na stężenie glukozy w surowicy krwi na czczo. Ze względu na działanie doustnych preparatów antykoncepcyjnych należy ściśle nadzorować kobiety ze stanem przedcukrzycowym lub cukrzycą, które przyjmują doustne preparaty antykoncepcyjne.
U małego odsetka kobiet przyjmujących doustne preparaty antykoncepcyjne występuje utrzymujące się podwyższone stężenie trójglicerydów w surowicy krwi (hipertriglicerydemia).
Ból głowy
W przypadku wystąpienia po raz pierwszy lub nasilenia migreny albo wystąpienia bólu głowy o nietypowym przebiegu, nawracającego, utrzymującego się lub ciężkiego należy przerwać stosowanie doustnego preparatu antykoncepcyjnego i zbadać przyczynę bólu głowy.
Nieregularne krwawienia
U kobiet przyjmujących doustne preparaty antykoncepcyjne, zwłaszcza podczas pierwszych trzech miesięcy ich stosowania mogą wystąpić krwawienia międzymiesiączkowe, plamienia i (lub) brak krwawienia. Należy określić, czy nie występuje inna przyczyna tych zaburzeń i w razie potrzeby przeprowadzić dodatkowe badania w celu wykluczenia nowotworu lub ciąży.
U niektórych kobiet po zakończeniu przyjmowania doustnych preparatów antykoncepcyjnych może wystąpić brak miesiączki lub rzadkie miesiączkowanie szczególnie w przypadkach, gdy takie zaburzenia występowały przed rozpoczęciem stosowania doustnych środków antykoncepcyjnych.
Plamiste przebarwienia skóry, głównie na twarzy (ostuda)
W rzadkich przypadkach u kobiet przyjmujących doustne preparaty antykoncepcyjne może wystąpić ostuda szczególnie u kobiet, u których ostuda występowała w ciąży. Kobiety ze skłonnością do ostudy podczas przyjmowania preparatu powinny unikać ekspozycji na słońce lub promieniowanie nadfioletowe. Ostuda często nie ustępuje całkowicie po odstawieniu preparatu.
Stosowanie podczas ciąży i w okresie karmienia piersią
Preparatu Cilest® nie należy stosować w okresie ciąży.
Wpływ na zdolność kierowania pojazdami mechanicznymi, obsługę maszyn i sprawność psychofizyczną
Preparat Cilest® nie ma wpływu na zdolność prowadzenia pojazdów mechanicznych i obsługiwania urządzeń mechanicznych w ruchu.
Oddziaływanie z innymi lekami (interakcje).
Na metabolizm doustnych preparatów antykoncepcyjnych mogą wpływać różne leki i preparaty ziołowe, w tym preparaty dziurawca zwyczajnego. Skuteczność preparatu w sposób istotny zmniejszają czynniki, które nasilają metabolizm i wydalanie substancji czynnych. Należą do nich czynniki pobudzające enzymy metabolizujące estrogeny, oraz czynniki wpływające na krążenie jelitowo-wątrobowe estrogenów. Zmniejszona skuteczność działania składnika estrogenowego doustnego preparatu antykoncepcyjnego może powodować plamienie, krwawienie międzymiesiączkowe lub nieskuteczność działania antykoncepcyjnego. Możliwe jest, że pobudzenie tych samych izoenzymów może prowadzić także do zmniejszenia stężenia składnika progestagenowego preparatu Cilest® we krwi. Znaczenie kliniczne mają leki i preparaty ziołowe, o których wiadomo, że wpływają pobudzająco na enzymy, które są odpowiedzialne za rozkład hormonów steroidowych zawartych w doustnych preparatach antykoncepcyjnych (np. dziurawiec zwyczajny, barbiturany, sól sodowa fenytoiny, a zwłaszcza ryfampicyna). Niektóre inhibitory proteazy i niektóre leki przeciw retrowirusom zwiększają (np. indinawir) lub zmniejszają (np. ritonawir) stężenie substancji czynnych złożonych hormonalnych preparatów antykoncepcyjnych we krwi.
Inny rodzaj interakcji stanowi zaburzenie krążenia jelitowo-wątrobowego estrogenów, które prowadzić może do przyspieszenia wydalania substancji czynnych i zmniejszenia skuteczności doustnych preparatów antykoncepcyjnych. Interakcję taką obserwuje się np., kiedy lek (np. cholestyramina) łączy się ze związkami sprzężonymi estrogenów z żółci albo, kiedy następuje osłabienie rozkładu związków sprzężonych przez bakterie jelitowe (np. po zastosowaniu niektórych antybiotyków - ampicyliny albo tetracykliny).
Zmniejszenie skuteczności działania antykoncepcyjnego stwierdzono przy jednoczesnym stosowaniu preparatu Cilest® i ryfampicyny oraz preparatów dziurawca zwyczajnego. Opisywano interakcje z topiramatem, barbituranami, fenylobutazonem, solą sodową fenytoiny, karbamazepiną. Możliwe jest wystąpienie interakcji z gryzeofulwiną, ampicyliną, (troglitazonem) i tetracyklinami.
Wpływ preparatu Cilest® na wyniki badań laboratoryjnych
Doustne preparaty antykoncepcyjne mogą wpływać na wyniki niektórych badań czynnościowych układu wydzielania wewnętrznego i wątroby oraz na wyniki badania krwi:
- Zwiększenie stężenia protrombiny oraz czynników II, VII, VIII, IX, X, XII oraz XIII; zmniejszenie stężenia antytrombiny 3; nasilenie wywołanej przez noradrenalinę agregacji płytek.
- Zwiększenie stężenia globuliny wiążącej hormony tarczycy (TBG), co prowadzi do zwiększenia całkowitego stężenia hormonów tarczycy we krwi, mierzonego jako jod związany z białkami (PBI), stężenie tyroksyny mierzone metodą chromatografii kolumnowej lub metodą radioimmunologiczną. Zmniejszenie wychwytu wolnej trijodotyroniny przez żywicę, co odpowiada zwiększeniu stężenia TBG. Stężenie wolnej tyroksyny pozostaje niezmienione.
- Może wystąpić zwiększenie stężenia innych białek wiążących w surowicy krwi.
- Zwiększenie stężenia globulin wiążących hormony płciowe co prowadzi do zwiększenia stężeń całkowitych hormonów płciowych we krwi. Niemniej jednak stężenia wolnych, czyli biologicznie czynnych hormonów zmniejszają się lub pozostają niezmienione.
- Może wystąpić zwiększenie stężenia frakcji cholesterolu lipoprotein o dużej gęstości (HDL) oraz stężenia całkowitego cholesterolu. Może wystąpić zwiększenie lub zmniejszenie stężenia frakcji cholesterolu lipoprotein o małej gęstości (LDL) przy zmniejszeniu wskaźnika LDL-C / HDL-C oraz nie zmienionym stężeniu triglicerydów. Wymienione efekty działania zależą od dawek estrogenu i progestagenu oraz rodzaju progestagenu.
- Może wystąpić pogorszenie tolerancji glukozy.
- Podczas stosowania doustnych preparatów antykoncepcyjnych może dojść do zmniejszenia stężenia kwasu foliowego w surowicy krwi. Może to mieć znaczenie kliniczne w przypadku, gdyby kobieta zaszła w ciążę wkrótce po zakończeniu stosowania doustnych preparatów antykoncepcyjnych.
Dawkowanie i sposób podania
Skuteczność działania doustnych preparatów antykoncepcyjnych
Przy stosowaniu dokładnie według zaleceń bez pominięcia jakiejkolwiek tabletki, prawdopodobieństwo zajścia w ciążę wynosi poniżej 1% (tzn. mniej niż 1 ciąża na 100 kobiet stosujących preparat przez rok). Średni wskaźnik niepowodzeń wynosi 5% w ciągu pierwszego roku stosowania. Prawdopodobieństwo zajścia w ciążę zwiększa się z każdą pominiętą tabletką w danym cyklu miesiączkowym.
Stosowanie u osób dorosłych
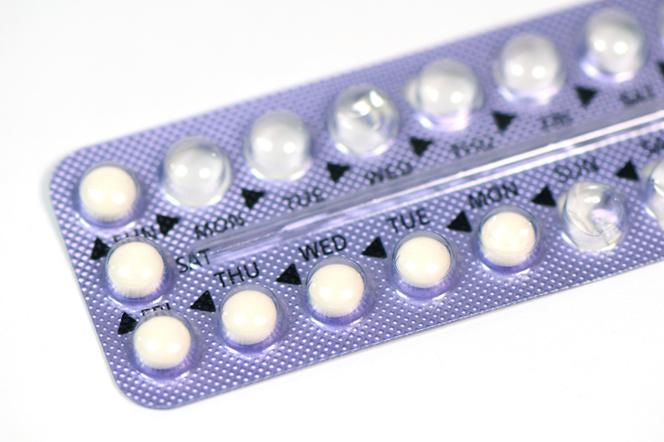
By osiągnąć maksymalną skuteczność działania antykoncepcyjnego tabletki preparatu Cilest® należy przyjmować dokładnie według zaleceń i w odpowiedniej kolejności, codziennie o tej samej porze, np. przed snem. Tabletki należy przyjmować codziennie bez przerwy w następujący sposób: Przyjmować jedną tabletkę raz na dobę popijając wodą, o tej samej porze dnia przez 21 dni. Po przyjęciu ostatniej tabletki, przez 7 dni nie należy przyjmować tabletek. W okresie nieprzyjmowania leku, zwykle po 2 do 4 dniach od przyjęcia ostatniej tabletki można spodziewać się wystąpienia krwawienia. Po zakończeniu tego 7-dniowego okresu należy rozpocząć nowy cykl przyjmowania tabletek preparatu Cilest®, także w przypadku, gdyby krwawienie nie wystąpiło lub nie zakończyło się.
W pierwszym cyklu stosowania, przyjmowanie preparatu należy rozpocząć w pierwszym dniu krwawienia miesiączkowego (w sposób opisany powyżej). Lek należy przyjmować popijając wodą, o tej samej porze dnia, przez 21 dni. Preparat Cilest® przyjmowany zgodnie z zaleceniami działa antykoncepcyjnie począwszy od pierwszego dnia przyjmowania, i w okresie 7 dni nieprzyjmowania tabletek (między kolejnymi opakowaniami preparatu).
Dzieci
Bezpieczeństwo stosowania oraz skuteczność preparatu Cilest® określono u kobiet w wieku rozrodczym. Leku nie należy stosować u dziewcząt przed rozpoczęciem miesiączkowania.
Osoby w wieku podeszłym
Nie zaleca się stosowania preparatu przez kobiety w okresie pomenopauzalnym.
Rozpoczęcie stosowania preparatu Cilest® u kobiet wcześniej przyjmujących inny doustny złożony (estrogenowo – progestagenowy) preparat antykoncepcyjny.
W przypadku przejścia z innego złożonego, doustnego preparatu antykoncepcyjnego, stosowanie preparatu Cilest® należy rozpocząć w okresie od 1 do 7 dni od przyjęcia ostatniej tabletki używanego w poprzednim cyklu preparatu antykoncepcyjnego. Przerwa między przyjęciem ostatniej tabletki preparatu poprzednio stosowanego a przyjęciem pierwszej tabletki preparatu Cilest® nie powinna być dłuższa niż 7 dni. W przypadku dłuższej niż 7 dni przerwy pomiędzy przyjęciem w poprzednim cyklu ostatniej tabletki antykoncepcyjnej a przyjęciem pierwszej tabletki preparatu Cilest® konieczne jest zastosowanie skutecznej, dodatkowej, niehormonalnej metody antykoncepcji. Należy stosować ją przez tydzień, tzn. do czasu przyjęcia siedmiu tabletek preparatu Cilest®.
Rozpoczęcie stosowania preparatu Cilest® u kobiet wcześniej przyjmujących inny doustny (zawierający wyłącznie progestagen) preparat antykoncepcyjny.
Przy przechodzeniu ze stosowania preparatu antykoncepcyjnego zawierającego wyłącznie progestagen, przyjmowanie preparatu Cilest® należy rozpocząć w pierwszym dniu po przyjęciu ostatniej tabletki poprzednio stosowanego preparatu. W okresie pierwszych 7 dni należy stosować dodatkową niehormonalną metodę antykoncepcji.
Stosowanie preparatu Cilest® po porodzie
Kobiety, które postanowiły nie karmić piersią mogą rozpocząć stosowanie doustnego preparatu antykoncepcyjnego, w tym preparatu Cilest® nie wcześniej niż po 3 tygodniach od dnia porodu (patrz Zaburzenia zakrzepowo-zatorowe i inne zaburzenia naczyniowe oraz Ciąża i okres karmienia piersią). W przypadku podjęcia decyzji rozpoczęcia stosowania preparatu Cilest® później niż 21 dni od porodu lekarz prowadzący może zdecydować, czy przez pierwsze 7 dni konieczne jest zastosowanie razem z preparatem Cilest® dodatkowej, niehormonalnej metody antykoncepcji, czy też należy poczekać z podaniem preparatu Cilest® do wystąpienia pierwszego krwawienia miesięcznego.
Stosowanie po poronieniu
Po poronieniu, które nastąpiło przed 20 tygodniem ciąży, można natychmiast rozpocząć przyjmowanie doustnych preparatów antykoncepcyjnych. Nie jest konieczne stosowanie dodatkowej metody antykoncepcji.
Po poronieniu, które nastąpiło w 20 tygodniu ciąży lub później stosowanie hormonalnych preparatów antykoncepcyjnych można rozpocząć w 21 dniu po poronieniu albo w pierwszym dniu pierwszego samoistnego krwawienia miesiączkowego - w zależności od tego, co nastąpi wcześniej. W ciągu pierwszych 7 dni pierwszego cyklu należy jednocześnie stosować niehormonalną metodę antykoncepcji. W wyjątkowych przypadkach, gdy występują wskazania do rozpoczęcia skutecznej metody antykoncepcji natychmiast po poronieniu przyjmowanie preparatu Cilest® należy rozpocząć w ciągu pierwszego tygodnia po poronieniu. Należy przy tym liczyć się z zwiększonym ryzykiem wystąpienia zaburzeń zakrzepowo-zatorowych w okresie bezpośrednio po poronieniu.
Postępowanie w razie nieprzyjęcia tabletek we właściwym czasie
W razie nie przyjęcia w odpowiednim czasie jednej tabletki (pomiędzy przyjęciem kolejnych tabletek nie powinno upływać więcej niż 24 godziny), należy przyjąć pominiętą tabletkę jak najszybciej po przypomnieniu sobie tego faktu. Nastepną tabletkę należy przyjąć w zaplanowanym czasie. Oznacza to, że w ciągu jednej doby mogą zostać przyjęte dwie tabletki.
W przypadku, gdy w ciągu pierwszego lub drugiego tygodnia cyklu pominięto przyjęcie dwóch tabletek należy przyjąć dwie tabletki w dniu, w którym przypomniano sobie o konieczności zastosowania preparatu oraz dwie tabletki w dniu następnym. Następnie należy przyjmować po jednej tabletce na dobę zgodnie z zaleceniem do momentu zużycia wszystkich tabletek w opakowaniu. Ponadto w okresie do dnia przyjęcia po kolei, codziennie, siódmej tabletki należy stosować dodatkową, skuteczną, niehormonalną metodę antykoncepcji.
W przypadku, gdy nie przyjęto dwóch tabletek w trzecim tygodniu stosowania preparatu, nie należy przyjmować kolejnych tabletek z tego opakowania, wyrzucić je i w tym samym dniu rozpocząć przyjmowanie tabletek z następnego opakowania. Ponadto, w okresie do dnia przyjęcia po kolei, codziennie, siódmej tabletki należy stosować dodatkową, skuteczną niehormonalną metodę antykoncepcji.
W przypadku, gdy nie przyjęto trzech tabletek w okresie pierwszych trzech tygodni stosowania preparatu, nie należy przyjmować kolejnych tabletek z tego opakowania, wyrzucić je i rozpocząć w tym samym dniu przyjmowanie tabletek z następnego opakowania. Ponadto, w okresie do dnia przyjęcia po kolei, codziennie siódmej tabletki należy stosować dodatkową, skuteczną niehormonalną metodę antykoncepcji.
Krwawienie międzymiesiączkowe lub plamienie
W przypadku wystąpienia krwawienia międzymiesiączkowego lub plamienia należy kontynuować stosowanie antykoncepcji. Wystąpienie krwawienia międzymiesiączkowego jest bardziej prawdopodobne przy stosowaniu preparatów hamujących jajeczkowanie (owulację) z małą zawartością estrogenu. Tego rodzaju krwawienie często ustępuje po kilku cyklach. W przypadku utrzymywania się krwawienia międzymiesiączkowego należy zgłosić się do ginekologa.
W przypadku gdyby w okresie nieprzyjmowania tabletek nie występowało krwawienie (tzw. krwawienie z odstawienia) należy nadal przyjmować preparat antykoncepcyjny. Jeżeli doustny preparat antykoncepcyjny był przyjmowany prawidłowo, brak krwawienia w okresie nieprzyjmowania tabletek nie musi wskazywać na ciążę. Niemniej jednak trzeba wykluczyć występowanie ciąży.
Postępowanie w razie wymiotów
W przypadku wystąpienia wymiotów w ciągu 3 godzin od momentu przyjęcia tabletki lub w razie utrzymywania się ciężkiej biegunki przez okres ponad 24 godzin skuteczność antykoncepcyjna preparatu może być zmniejszona. Jeżeli wymioty lub biegunka ustąpią szybko skuteczne działanie antykoncepcyjne będzie zachowane, o ile tego samego dnia przyjęta będzie druga tabletka preparatu Cilest®. W razie występowania wymiotów lub biegunki trwających przez 24 godziny lub dłużej działanie antykoncepcyjne może być zmniejszone i należy zastosować dodatkową, niehormonalną metodę antykoncepcji do dnia przyjęcia kolejno (codziennie) siedmiu tabletek.
Przedawkowanie
Nie opisano zagrażających życiu objawów spowodowanych przedawkowaniem doustnych preparatów antykoncepcyjnych. Przedawkowanie może być przyczyną nudności i wymiotów a u dziewcząt krwawienia z dróg rodnych. Nie ma antidotum i należy zastosować leczenie objawowe.
Działania niepożądane
Podczas stosowania doustnych preparatów antykoncepcyjnych zgłaszano poniżej wymienione działania niepożądane (patrz Specjalne ostrzeżenia i środki ostrożności dotyczące stosowania).
- Układ sercowo-naczyniowy: nadciśnienie tętnicze, zawał mięśnia sercowego, zaburzenia krążenia mózgowego, zakrzepica żył głębokich, zaburzenia zakrzepowo-zatorowe tętnic, zatorowość płucna i inne zatory.
- Guzy: łagodne guzy wątroby, złośliwe guzy wątroby, rak szyjki macicy, rak piersi.
-Wątroba i drogi żółciowe: zastój żółci (cholestaza) wewnątrzwątrobowa, kamica żółciowa.
- Różne: ciężki ból głowy, migrena, uszkodzenie nerwu wzrokowego.
Inne działania niepożądane
- Układ sercowo-naczyniowy: niewielkie podwyższenie ciśnienia tętniczego, obrzęki.
- Układ rozrodczy: krwawienia międzymiesiączkowe, plamienie, brak miesiączki, brak krwawienia z odstawienia, zmiany nasilenia krwawienia miesiączkowego, zwiększenie wielkości włókniakomięśniaków macicy, kandydioza pochwy, nasilenie nadżerki szyjki macicy i wydzielania przez gruczoły szyjkowe.
- Piersi: tkliwość, mlekotok, ból, powiększenie, zmniejszenie wydzielania mleka przy stosowaniu bezpośrednio po porodzie.
- Przewód pokarmowy: nudności, wymioty, kurcze brzucha, wzdęcia, zapalenie jelita grubego. Skóra: rumień guzowaty, wysypka, ostuda, rumień wielopostaciowy, trądzik, łojotok, łysienie, nadmierne owłosienie (hirsutyzm, hipertrichosis), pemfigoid (opryszczka ciężarnych), przebarwienia, które mogą nie ustąpić po odstawieniu, wykwity krwotoczne.
- Wątroba i drogi żółciowe: żółtaczka spowodowana zastojem żółci (cholestatyczna), zespół Budd-Chiari.
- Oczy: zmiana krzywizny rogówki (zmacerowanie), nietolerancja szkieł kontaktowych, zaćma. Ośrodkowy układ nerwowy: ból głowy, zmiany nastroju, depresja, drażliwość, pląsawica. Zaburzenia metaboliczne: zatrzymanie płynów, zmiany masy ciała (zwiększenie lub zmniejszenie), upośledzenie tolerancji glukozy, zmiany łaknienia.
- Inne: zmiany popędu płciowego (libido), zespół napięcia przedmiesiączkowego, tymczasowa bezpłodność przemijająca po odstawieniu preparatu.
- Układ moczowy: zaburzenie czynności nerek, zespół hemolityczno-mocznicowy.
O występowaniu wymienionych lub innych działań niepożądanych należy poinformować lekarza.
Nie należy stosować preparatu po upływie terminu ważności
Sposób przechowywania
Przechowywać w oryginalnym opakowaniu.
Przechowywać w temperaturze do 25 °C.
Przechowywać w miejscu niedostępnym dla dzieci.
Dostępne opakowania
Opakowanie bezpośrednie
Blister zawierający 21 tabletek
Opakowanie zbiorcze
Blistry zapakowane są w kartoniki.
Jeden kartonik zawiera 1 albo 3 blistry preparatu Cilest® w tabletkach.
Podmiot odpowiedzialny
Janssen – Cilag International NV
Turnhoutseweg 30
B – 2340 Beerse
Belgia
Wytwórca,u którego zwalniana jest seria produktu leczniczego
Janssen Pharmaceutica NV
Turnhoutseweg 30
B – 2340 Beerse
Belgia
W celu uzyskania bardziej szczegółowych informacji należy zwrócić się do przedstawiciela podmiotu odpowiedzialnego:
Janssen-Cilag Polska Sp. z o.o.
ul. Iłżecka 24
02-135 Warszawa
Data sporządzenia ulotki: 3.10.2007 r.
UWAGA! Ulotka informacyjna dla pacjenta dołączona jest do opakowania leku. Zawiera informacje przeznaczone dla pacjenta na temat właściwego stosowania leku.