- Krakowscy naukowcy odkryli, dlaczego u niektórych osób z prawidłowym poziomem cukru we krwi dochodzi do uszkodzeń naczyń krwionośnych.
- Badania wykazały, że kluczową rolę odgrywa tu enzym, który wpływa na metabolizm glukozy w komórkach.
- To przełomowe odkrycie może prowadzić do nowych metod leczenia i zapobiegania powikłaniom naczyniowym.
- Jakie są konsekwencje tego odkrycia dla medycyny i pacjentów?
Gdy cukier nie jest winny, a naczynia i tak chorują
Cukrzyca kojarzy się przede wszystkim z chronicznie podwyższonym poziomem glukozy we krwi i wynikającymi z tego uszkodzeniami narządów. Tymczasem istnieje rzadka, genetycznie uwarunkowana jej odmiana – HNF1A-MODY – w której nawet dobrze wyrównani metabolicznie pacjenci nie są wolni od poważnych powikłań naczyniowych. Zjawisko to od lat stanowiło zagadkę dla klinicystów. Teraz, dzięki badaniom prowadzonym na Uniwersytecie Jagiellońskim w Krakowie, zaczyna być rozumiane na poziomie molekularnym.
Zespół pod kierunkiem dr hab. Neli Kachamakovej-Trojanowskiej z Małopolskiego Centrum Biotechnologii UJ opublikował wyniki swoich badań w prestiżowym czasopiśmie „Genome Medicine". Praca, zatytułowana "Integrated transcriptome and proteome analyses unveil cytoskeletal alterations in an endothelial model of monogenic diabetes", rzuca nowe światło na mechanizmy, które mogą tłumaczyć, dlaczego część pacjentów z monogenną cukrzycą pozostaje narażona na choroby sercowo-naczyniowe niezależnie od tego, jak skutecznie kontrolują swoją glikemię.
Śródbłonek pod lupą. To był klucz do rozwiązania zagadki
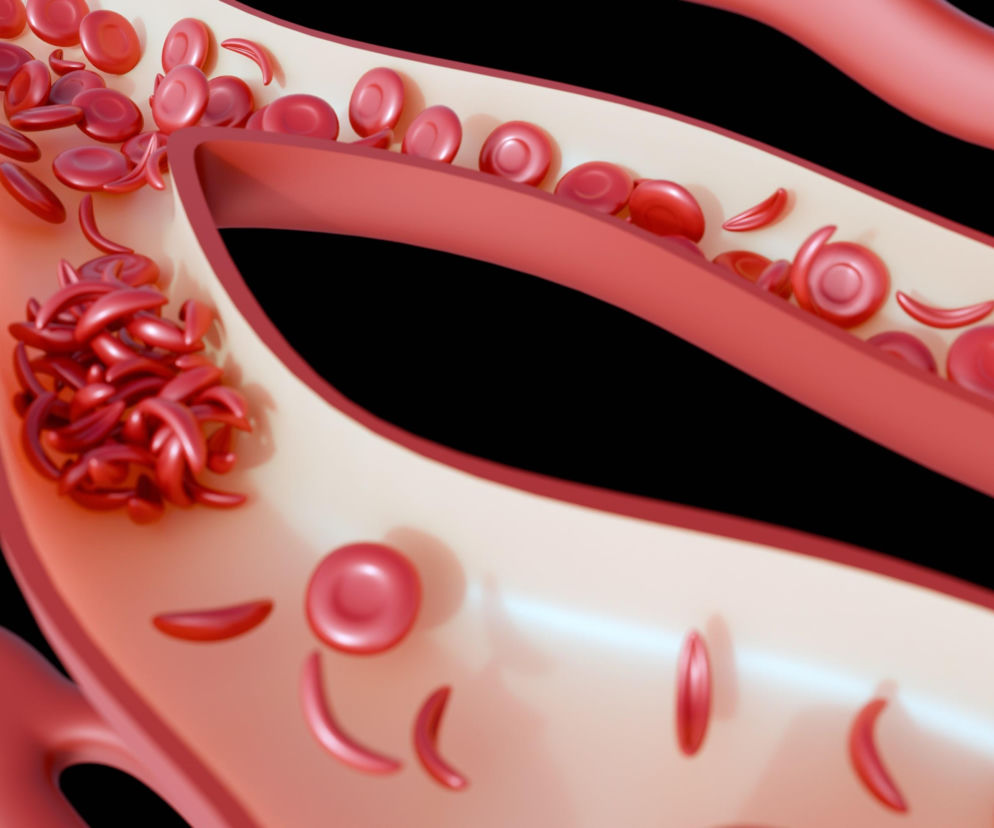
Przedmiotem badań były komórki śródbłonka – cienkiej, jednokomórkowej wyściółki pokrywającej wnętrze naczyń krwionośnych. To właśnie one pełnią funkcję swoistej bariery i regulatora między krwią a tkankami: kontrolują przepływ substancji odżywczych, modulują stan zapalny i decydują o elastyczności naczyń. W HNF1A-MODY gen HNF1A ulega mutacji – a jego prawidłowe działanie jest niezbędne nie tylko dla komórek trzustki wytwarzających insulinę, lecz, jak się okazuje, również dla komórek naczyniowych.
Wykorzystując zaawansowane analizy genomowe (transkryptomiczne) oraz proteomiczne, krakowscy naukowcy porównali komórki śródbłonka z mutacjami HNF1A z komórkami zdrowymi. Odkryte różnice okazały się znaczące i wielowymiarowe – obejmowały zaburzenia metabolizmu komórkowego, nieprawidłową organizację cytoszkieletu oraz zmiany w środowisku zewnątrzkomórkowym.
Glikokaliks – ochronna warstwa, której brakuje
Jednym z najbardziej wymownych odkryć jest systematyczne zmniejszenie grubości glikokaliksu – struktury, którą można wyobrazić sobie jako ochronny „dywan" z cukrów i białek pokrywający powierzchnię komórek śródbłonka od strony światła naczynia. Glikokaliks nie jest bierną powłoką – aktywnie uczestniczy w regulacji przepuszczalności naczyń, hamowaniu procesów zapalnych i zapewnieniu prawidłowego przepływu krwi. Jego uszkodzenie lub redukcja to jeden z wczesnych sygnałów dysfunkcji śródbłonka, wiązany z rozwojem miażdżycy i innych chorób układu sercowo-naczyniowego.
W komórkach z mutacją HNF1A warstwa ta była wyraźnie cieńsza – i to niezależnie od poziomu glukozy w środowisku hodowlanym. To kluczowe spostrzeżenie: zmiany nie były wtórne wobec hiperglikemii, lecz wynikały bezpośrednio z defektu genetycznego.
Komórka, która nie potrafi stać w miejscu
Badanie ujawniło również zaburzenia w organizacji cytoszkieletu komórek śródbłonkowych, a konkretnie – struktury zbudowanej z aktyny, białka odpowiedzialnego za kształt i mechaniczną stabilność komórki. Komórki z mutacją HNF1A wykazywały nieprawidłowe rozmieszczenie włókien aktynowych, co przekładało się na zwiększoną zdolność do migracji. Brzmi to niewinnie, ale w kontekście biologii naczyniowej oznacza poważny problem: komórki, które zbyt łatwo się przemieszczają, gorzej utrzymują integralność ściany naczynia i mogą przyczyniać się do jej przeciekania lub nieprawidłowej przebudowy.
Co istotne dla wiarygodności wyników, podobne zmiany zaobserwowano zarówno w komórkach śródbłonka pochodzących z indukowanych pluripotencjalnych komórek macierzystych (hiPSC), jak i w komórkach pierwotnych, w których wyciszono gen HNF1A metodami eksperymentalnymi. To podwójne potwierdzenie sprawia, że związek przyczynowo-skutkowy między mutacją a dysfunkcją śródbłonka jest trudny do podważenia.
Pierwsze takie dowody. Co z nich wynika?
Jak podkreślają autorzy, opisane obserwacje stanowią pierwsze bezpośrednie dowody na to, że mutacje w genie HNF1A mogą upośledzać funkcję komórek śródbłonka w sposób niezależny od glikemii. Ta dysfunkcja może wyjaśniać kliniczny paradoks, z którym mierzą się lekarze: dlaczego pacjenci z HNF1A-MODY – nawet ci wzorowo prowadzeni pod względem wyrównania metabolicznego – rozwijają retinopatię cukrzycową i inne powikłania naczyniowe.
– Badania te otwierają nowe możliwości w zrozumieniu powikłań naczyniowych związanych z cukrzycą i wskazują, że skuteczne leczenie pacjentów z monogennymi formami cukrzycy wymaga podejścia wykraczającego poza samą kontrolę glikemii – wyjaśnia dr hab. Neli Kachamakova-Trojanowska z Małopolskiego Centrum Biotechnologii UJ, wiodąca autorka badania.
Szeroka współpraca i finansowanie
Badanie nie powstałoby bez interdyscyplinarnego wysiłku. W projekcie uczestniczyli naukowcy z Wydziału Fizyki, Astronomii i Informatyki Stosowanej UJ, Wydziału Biochemii, Biofizyki i Biotechnologii UJ, Narodowego Centrum Promieniowania Synchrotronowego SOLARIS oraz Collegium Medicum Uniwersytetu Jagiellońskiego. Finansowanie zapewniły granty OPUS i SONATA-BIS Narodowego Centrum Nauki, przyznane dr hab. Neli Kachamakovej-Trojanowskiej.
Wyniki badań zostały opublikowane w czasopiśmie „Genome Medicine" – jednym z czołowych periodyków z zakresu genomiki klinicznej i medycyny molekularnej. Odkrycia krakowskiego zespołu mogą w perspektywie otworzyć drogę do nowych strategii terapeutycznych, w których ochrona śródbłonka naczyniowego stanie się integralnym elementem opieki nad pacjentami z rzadkimi postaciami cukrzycy – niezależnie od wartości hemoglobiny glikowanej.
Źródło: Materiały prasowe UJ