Spis treści
- Nowa era onkologii: organizm sam staje się "apteką"
- Biologiczny "haker", czyli jak powstaje chimeryczny receptor
- Laboratorium zamiast fabryki leków. Proces produkcji CAR-T
- Spektakularne sukcesy i cena nadziei
- Ciemna strona medalu: CRS i neurotoksyczność
- Refundacja CAR-T w Polsce: Gdzie jesteśmy w 2026 roku?
- Mapa nadziei – ośrodki CAR-T w Polsce
- Przyszłość: Czy CAR-T pokona raka piersi i płuc?
Nowa era onkologii: organizm sam staje się "apteką"
Przez dziesięciolecia fundamentem onkologii była „wielka trójka”: chirurgia, radioterapia i chemioterapia. Choć skuteczne, metody te często przypominają strzelanie z armaty do muchy – niszczą komórki nowotworowe, ale przy okazji dewastują zdrowe tkanki. Terapia CAR-T (chimeric antigen receptor T-cell therapy) wywraca ten paradygmat do góry nogami. To nie jest zwykły lek w tabletce czy kroplówce. To proces, w którym pacjent staje się jednocześnie dawcą surowca i biorcą wysoce spersonalizowanego bioproduktu.
CAR-T to połączenie immunoterapii, inżynierii genetycznej i medycyny komórkowej. Istotą tej metody jest wykorzystanie limfocytów T – naturalnych „żołnierzy” naszego układu odpornościowego, których zadaniem jest eliminacja patogenów. W przebiegu nowotworu limfocyty te często stają się „ślepe” na komórki rakowe, które wykształcają mechanizmy maskujące. Technologia CAR-T zdejmuje tę "opaskę z oczu" układu immunologicznego, programując go na nowo.
Biologiczny "haker", czyli jak powstaje chimeryczny receptor
Słowo „chimeryczny” w nazwie terapii nie jest przypadkowe. Nawiązuje do mitycznej Chimery, istoty złożonej z części różnych zwierząt. W świecie medycyny oznacza to, że receptor wszczepiony do limfocytu T łączy w sobie dwie kluczowe funkcje układu odpornościowego:
- Odpowiedź humoralną (przeciwciała): zdolność do precyzyjnego rozpoznawania konkretnego „odcisku palca” nowotworu (antygenu).
- Odpowiedź komórkową (limfocyty cytotoksyczne): potężną siłę rażenia, która fizycznie niszczy namierzoną komórkę.
Dzięki modyfikacji genetycznej limfocyt zyskuje receptor CAR, który działa jak precyzyjny GPS. Gdy tylko napotka on na swojej drodze antygen (w przypadku białaczek to najczęściej CD19), natychmiast inicjuje proces niszczenia intruza.
Laboratorium zamiast fabryki leków. Proces produkcji CAR-T
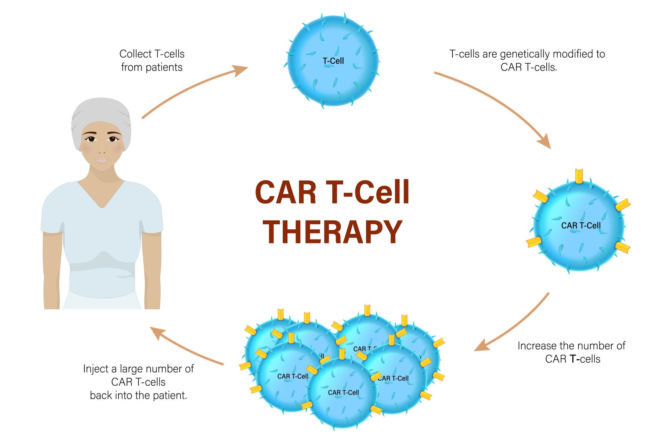
Produkcja tego „żywego leku” to logistyczny majstersztyk, który trwa zazwyczaj od kilku do kilkunastu dni. Proces ten można podzielić na precyzyjne etapy:
1. Pobranie materiału (Leukafereza)
Wszystko zaczyna się w certyfikowanym ośrodku medycznym. Pacjent zostaje podłączony do separatora komórkowego, który odfiltrowuje z jego krwi limfocyty, a pozostałe składniki (osocze, erytrocyty) oddaje z powrotem do krwiobiegu. Ten etap przypomina procedurę oddawania osocza.
2. Transport w warunkach kriogenicznych
Pobrane komórki są zamrażane i wysyłane do specjalistycznego laboratorium (często znajdującego się w innym kraju, np. w Niemczech czy USA, choć w Polsce powstają już własne centra produkcyjne).
3. Przeprogramowanie genetyczne
To serce całej procedury. Za pomocą wektorów wirusowych (bezpiecznych fragmentów wirusa, pełniących rolę „taksówki”) do DNA limfocytów wprowadza się instrukcję budowy receptora CAR. Od tego momentu komórka jest już „zaprogramowanym zabójcą” nowotworu.
4. Ekspansja, czyli budowa armii
Pojedyncze zmodyfikowane komórki to za mało. W bioreaktorach poddaje się je stymulacji, by zaczęły się gwałtownie dzielić. Celem jest uzyskanie milionów kopii, które po powrocie do organizmu pacjenta będą w stanie zdominować masę nowotworową.
5. Kontrola jakości i infuzja
Po serii rygorystycznych testów bezpieczeństwa, komórki wracają do szpitala. Pacjent przechodzi krótką chemioterapię (tzw. limfodeplecję), która ma „zrobić miejsce” w organizmie dla nowych jednostek. Następnie podaje się je w formie zwykłej kroplówki.
i
Spektakularne sukcesy i cena nadziei
Symbolem sukcesu CAR-T stała się Emily Whitehead. W 2012 roku, jako siedmiolatka, była pierwszą na świecie osobą, u której zastosowano tę metodę w walce z nawrotową ostrą białaczką limfoblastyczną (ALL). Lekarze nie dawali jej szans, a standardowe metody zawiodły. Dziś Emily jest zdrową, dorosłą kobietą, a w jej organizmie wciąż krążą komórki CAR-T, pełniąc rolę dożywotniej straży przybocznej.
W Polsce przełom nastąpił w 2017 roku, kiedy FDA zatwierdziła preparat tisagenlecleucel. Obecnie na rynku dostępnych jest kilka preparatów, w tym aksykabtagen cyloleucel. Terapia każdym z nich to koszt rzędu 1 miliona złotych (lub więcej, wliczając koszty hospitalizacji i procedur towarzyszących). To właśnie wysoka cena oraz konieczność posiadania kosmicznie zaawansowanej infrastruktury sprawiły, że przez lata CAR-T była terapią niemal nieosiągalną.
Ciemna strona medalu: CRS i neurotoksyczność
CAR-T to nie jest „cudowna pigułka” bez wad. Gwałtowność, z jaką zmodyfikowane komórki atakują nowotwór, wywołuje w organizmie prawdziwą burzę.
- Zespół uwalniania cytokin (CRS): To najczęstsze powikłanie. Kiedy miliony limfocytów jednocześnie atakują raka, wydzielają ogromne ilości cytokin – cząsteczek sygnałowych układu odpornościowego. Skutkiem jest stan przypominający ciężką sepsę: gorączka powyżej 40 stopni, dreszcze, spadki ciśnienia i niewydolność wielonarządowa. Choć brzmi to groźnie, współczesna medycyna radzi sobie z CRS za pomocą leków immunosupresyjnych.
- ICANS (Zaburzenia neurologiczne): Niektórzy pacjenci doświadczają obrzęku mózgu, utraty zdolności pisania, czytania czy mówienia (afazja). Choć większość tych objawów mija bez śladu po kilku dniach, odnotowano pojedyncze przypadki śmiertelne, co podkreśla wagę leczenia w ośrodkach o najwyższym stopniu referencyjności.
Refundacja CAR-T w Polsce: Gdzie jesteśmy w 2026 roku?
Polska poczyniła ogromne postępy w dostępie do technologii CAR-T. Od pamiętnego września 2021 roku, kiedy zrefundowano pierwszą terapię dla dzieci, lista wskazań systematycznie rośnie. Według stanu na luty 2026 r., refundacja obejmuje:
- Ostrą białaczkę limfoblastyczną (ALL) u dzieci i dorosłych do 25. roku życia (preparat tisagenlecleucel).
- Chłoniaka rozlanego z dużych komórek B (DLBCL) u pacjentów dorosłych, u których zawiodły co najmniej dwie linie leczenia standardowego.
- Chłoniaka z komórek płaszcza (MCL) oraz niektóre postacie chłoniaka grudkowego.
- Pojawiające się programy wczesnego dostępu dla pacjentów ze szpiczakiem mnogim.
Do 2025 roku pozytywnie rozpatrzono ponad 305 wniosków o refundację, co pokazuje skalę potrzeb. Eksperci podkreślają, że kluczem do sukcesu jest nie tylko pieniądz, ale i sieć akredytowanych placówek.
Mapa nadziei – ośrodki CAR-T w Polsce
Pacjenci nie muszą już szukać ratunku za granicą. Certyfikowane ośrodki działają m.in. w:
- Warszawie (UCK WUM, Narodowy Instytut Onkologii, Instytut Hematologii i Transfuzjologii),
- Gliwicach (Narodowy Instytut Onkologii),
- Poznaniu (Klinika Hematologii UM),
- Wrocławiu (Klinika „Przylądek Nadziei” dla dzieci oraz ośrodki dla dorosłych),
- Gdańsku, Szczecinie, Łodzi, Bydgoszczy i Lublinie.
Przyszłość: Czy CAR-T pokona raka piersi i płuc?
Obecnie technologia CAR-T najlepiej radzi sobie z nowotworami „płynnymi”, czyli takimi, gdzie komórki rakowe krążą we krwi lub chłonce. Największym wyzwaniem dla naukowców są guzy lite (np. rak płuca, trzustki czy piersi). Są one otoczone swoistym „pancerzem” (mikrośrodowiskiem nowotworowym), który jest nieprzyjazny dla limfocytów T.
W fazie badań klinicznych jest obecnie około 300 projektów. Naukowcy testują tzw. „pancerne CAR-T”, które potrafią przełamywać bariery guza litego, a także terapie wykorzystujące komórki NK (Natural Killers) – jeszcze szybsze i bezpieczniejsze w działaniu. Fascynującym kierunkiem jest też zastosowanie CAR-T w chorobach autoimmunologicznych (np. toczeń) oraz w ciężkiej astmie, gdzie zmodyfikowane komórki mogłyby „uspokoić” nadreaktywny układ odpornościowy.