Transplantacja (przeszczep) szpiku kostnego: wskazania, przebieg, powikłania
Transplantacja (przeszczep) szpiku kostnego to najskuteczniejsza metoda leczenia białaczki. Zdrowy szpik podany pacjentowi odtwarza tkanki krwiotwórcze w jego organizmie. Ale potrzebny jest dawca szpiku - człowiek, który będzie chciał dobrowolnie poddać się niezbyt skomplikowanej procedurze medycznej. Jakie są wskazania do wykonania przeszczepu szpiku? Jak przebiega procedura? Jakie mogą wystąpić powikłania?
Spis treści
- Transplantacja (przeszczep) szpiku kostnego: rodzaje
- Transplantacja (przeszczep) szpiku kostnego: dobór dawcy
- Transplantacja szpiku: przygotowanie dawcy do zabiegu
- Transplantacja szpiku: przygotowanie pacjenta do zabiegu
- Transplantacja szpiku: pobieranie komórek do przeszczepu
- Transplantacja szpiku: wskazania do przeszczepu
- Najczęstsze wskazania do auto- i allotransplantacji
- Transplantacja szpiku kostnego: przebieg
- Transplantacja (przeszczep) szpiku kostnego: powikłania
- Odrzucenie przeszczepianego szpiku kostnego
- Rokowanie pacjentów poddanych transplantacji
Transplantacja (przeszczep) szpiku kostnego to zabieg wykonywany w warunkach szpitalnych, polegający na przeszczepieniu choremu macierzystych komórek krwiotwórczych. Ich zadaniem jest odbudowanie uszkodzonego w przebiegu choroby nienowotworowej lub nowotworowej układu krwiotwórczego chorego.
Macierzyste komórki krwiotwórcze można pozyskać nie tylko ze szpiku kostnego, ale także wyizolować z krwi obwodowej lub z krwi pępowinowej.
Ze względu na pochodzenie pobieranych komórek, wyróżniamy 3 rodzaje transplantacji:
- przeszczepienie autogeniczne (dawcą komórek macierzystych jest sam chory)
- przeszczepienie syngeniczne (czyli izogeniczne, gdy dawcą komórek macierzystych jest jednojajowy brat bliźniak chorego)
- przeszczepienie allogeniczne (dawcą komórek macierzystych jest osoba niespokrewniona lub spokrewniona, lecz nie będąca bliźniakiem jednojajowym biorcy)
Transplantacja (przeszczep) szpiku kostnego: rodzaje
Podział transplantacji szpiku kostnego ze względu na pochodzenie przeszczepianego materiału:
PRZESZCZEPIENIE AUTOGENICZNE (auto-HSCT, ang. auto- hematopoietic stem cell transplantation)
To zabieg polegający na transplantacji pacjentowi jego własnych macierzystych komórek krwiotwórczych, pobranych od niego przed zastosowaniem leczenia mielosupresyjnego, czyli niszczącego szpik kostny.
Zalety przeszczepienia autogenicznego:
- daje możliwość zastosowania leczenia mieloablacyjnego, z wykorzystaniem bardzo dużych dawek chemioterapii lub radioterapii; efektem takiej terapii jest całkowite, nieodwracalne zniszczenie szpiku kostnego, w którym toczy się proces nowotworowy; taki model terapii jest korzystny u pacjentów, zmagających się ze schorzeniami podatnymi na wysokie dawki cytostatyków
- niskie ryzyko poważnych powikłań po transplantacji; choroba przeszczep przeciwko gospodarzowi (GVHD, ang. graft versus host disease) nie jest spotykana, ponieważ pacjentowi przeszczepiane są jego własne macierzyste komórki krwiotwórcze pobrane wcześniej
- brak ryzyka odrzucenia przeszczepu, ponieważ przeszczepiane są tkanki własne pacjenta
- brak konieczności stosowania leczenia immunosupresyjnego po transplantacji
- górna granica wieku biorców to 70. rok życia, natomiast do ostatecznej kwalifikacji do zabiegu bierze się pod uwagę nie tylko wiek chorego, ale także jego stan ogólny, występowanie chorób towarzyszących oraz zaawansowanie choroby nowotworowej
Wady przeszczepienia autogenicznego:
- metoda leczenia stosowana u pacjentów z guzem nowotworowym o małej masie i niskim zaawansowaniu choroby - w przeciwnym wypadku istnieje ryzyko niedostatecznego oczyszczenia przeszczepianego materiału z komórek nowotworowych i niezamierzone, ponowne ich wszczepienie, co może to skutkować nawrotem choroby
- nie występuje korzystna reakcja przeszczep przeciwko białaczce (GvL, ang. graft versus leukemia)
- istnieje wysokie ryzyko nawrotu choroby (około 45%)
PRZESZCZEPIENIE IZOGENICZNE (SYNGENICZNE)
To zabieg, który opiera się na transplantacji pacjentowi macierzystych komórek krwiotwórczych pobranych od jego brata bliźniaka. Bardzo istotne jest, aby rodzeństwo było identyczne pod względem genetycznym, czyli musi pochodzić z ciąży bliźniaczej jednojajowej (homozygotycznej).
PRZESZCZEPIENIE ALLOGENICZNE (allo-HSCT)
To zabieg, w którym przeszczep pochodzi od osoby, która nie jest bliźniakiem jednojajowym chorego. Dawca komórek macierzystych musi być zgodny z biorcą w zakresie antygenów HLA, może być z nim spokrewniony, bądź nie.
Obecnie zdecydowana większość transplantacji wykonywana jest w wykorzystaniem materiału pobranego od dawców niespokrewnionych.
Zalety przeszczepienia allogenicznego:
- umożliwia zastosowanie wcześniejszego leczenia chemio- lub radioterapeutycznego w dawkach, które spowodują całkowite zniszczenie zmienionego chorobowo szpiku kostnego, podobnie jak przeszczep autogeniczny
- przeszczepiany jest szpik od zdrowego dawcy, nie ma więc ryzyka zanieczyszczenia materiału przeszczepowego komórkami nowotworowymi i wznowy choroby
- występować może korzystna reakcja przeszczep przeciwko białaczce (GvL)
- istnieje niewielkie ryzyko nawrotu choroby (ok. 10%)
Wady przeszczepienia allogenicznego:
- wykonywany u osób do ok. 60. roku życia
- w związku z przeszczepianiem obcych tkanek i komórek pobranych od dawcy, w organizmie biorcy mogą wykształcić się zagrażające życiu powikłania; aż 10-30% chorych poddanych zabiegowi prezentuje reakcje niepożądane, do których należy przede wszystkim choroba przeszczep przeciwko gospodarzowi (GvHD) czy infekcje oportunistyczne
- znalezienie zgodnego dawcy może przysporzyć trudności
- w związku z przeszczepianiem obcych tkanek istnieje ryzyko odrzucenia przeszczepu
- konieczność stosowania leczenia immunosupresyjnego po transplantacji
Transplantacja (przeszczep) szpiku kostnego: dobór dawcy
Dobór dawcy do przeszczepu allogenicznego szpiku dotyczy głównego układu zgodności tkankowej (MHC, ang. major histocompatibility complex), który obejmuje wiele genów kodujących ludzkie antygeny leukocytarne (HLA, ang. human leukocyte antigens).
Właściwy dobór dawcy jest kluczowy dla powodzenia zabiegu. W przeciwnym razie istnieje wysokie prawdopodobieństwo wystąpienia wielu zagrażających życiu biorcy powikłań, jak choroba przeszczep przeciwko gospodarzowi (komórki pochodzące od dawcy rozpoznają tkanki biorcy jako obce i je niszczą), czy odrzucenie przeszczepu.
Warto zaznaczyć, że:
- nie jest wymagana zgodność grup krwi pomiędzy dawcą a biorcą
- nie jest określona górna granica wieku, powyżej której nie można być dawcą krwiotwórczych komórek macierzystych
- biorca i dawca przeszczepu nie muszą być jednakowej płci, nie ma przeciwwskazań odnośnie przeszczepiania szpiku kobiety mężczyźnie i odwrotnie
Zazwyczaj dawcą szpiku jest osoba spokrewniona, najczęściej rodzeństwo chorego, ponieważ istnieje wtedy najwyższa szansa na pełną zgodność w zakresie HLA z biorcą.
W sytuacji, w której dla biorcy nie znaleziono zgodnego antygenowo dawcy rodzinnego, konieczne jest rozpoczęcie poszukiwania dawcy niespokrewnionego. Umożliwia to światowy rejestr ochotników, którzy zdeklarowali gotowość do oddania komórek krwiotwórczych.
Transplantacja szpiku: przygotowanie dawcy do zabiegu
Przed pobraniem szpiku od dawcy, lekarz musi mieć pewność że jest on zdrowy, a w jego organizmie nie rozwija się infekcja, ani proces nowotworowy. Wymaganie jest wykonanie:
- szczegółowych badań laboratoryjnych krwi
- badania elektrokardiograficznego (EKG)
- badania radiologicznego klatki piersiowej
- USG jamy brzusznej
Co więcej, u dawcy należy wykluczyć zakażenie ludzkim wirusem niedoboru odporności (HIV), wirusem zapalenia wątroby, wirusem cytomegalii (CMV) oraz wirusem Epsteina-Barr (EBV).
Transplantacja szpiku: przygotowanie pacjenta do zabiegu
Każdy rodzaj przeszczepienia krwiotwórczych komórek macierzystych związany jest z koniecznością stosowania leków obniżających odporność biorcy, dlatego tak ważne jest wykluczenie wszelkich możliwych źródeł infekcji i dobry stan ogólny pacjenta przed rozpoczęciem zabiegu.
Kwalifikacja do transplantacji powinna obejmować między innymi:
- dokładną ocenę stadium nowotworu
- wykonanie szczegółowych badań laboratoryjnych celem oceny funkcji wątroby oraz nerek
- zbadanie wydolności serca i płuc
- wykluczenie zakażeń wirusami HIV, CMV, EBV oraz wirusem zapalenia wątroby
Nie należy zapominać o kontrolnej wizycie u stomatologa, lekarza specjalisty ginekologa oraz lekarza specjalisty laryngologa.
Transplantacja szpiku: pobieranie komórek do przeszczepu
Macierzyste komórki krwiotwórcze pobierać można ze szpiku kostnego, krwi obwodowej lub krwi pępowinowej.
Komórki pochodzące ze szpiku kostnego dawcy pobierane są w warunkach bloku operacyjnego, w znieczuleniu ogólnym.
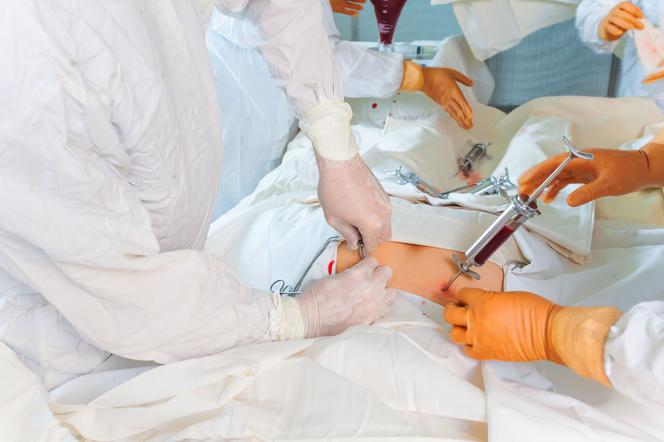
Zabieg polega na wielokrotnym nakłuwaniu igłą kości miednicy dawcy (dokładnie tylnego, górnego kolca biodrowego).
Pobrać należy około 15-20ml/kg masy ciała biorcy szpiku kostnego, czyli około 1-1,5 litra.
Dopiero w takiej ilości materiału znajdować będzie się odpowiednia ilość komórek macierzystych do odbudowy szpiku biorcy (powyżej lub równo 2x106/kg masy ciała biorcy).
Transplantacja szpiku: wskazania do przeszczepu
Wskazania do transplantacji macierzystych komórek krwiotwórczych zgodnie z rekomendacjami Europejskiej Grupy Przeszczepiania Krwi i Szpiku.
Nowotwory układu krwiotwórczego i chłonnego
- ostra białaczka szpikowa
- ostra białaczka limfoblastyczna
- zespoły mielodysplastyczne
- przewlekła białaczka szpikowa
- samoistne włóknienie szpiku
- chłoniak rozlany z dużych komórek B
- chłoniak Burkitta
- chłoniak z komórek płaszcza
- chłoniak grudkowy
- przewlekła białaczka limfocytowa
- chłoniaki z limfocytów T
- chłoniak Hodgkina
- szpiczak plazmocytowy
Nowotwory lite:
- nowotwory z komórek rozrodczych
- rak jasnokomórkowy nerki
- neuroblastoma
- rak jajnika
Choroby nienowotworowe:
- niedokrwistość aplastyczna
- nocna napadowa hemoglobinuria
- niedokrwistość Fanconiego
- niedokrwistość Blackfana i Diamonda
- talasemia major
- niedokrwistość sierpowata
- wrodzone zaburzenia metaboliczne
- choroby autoimmunologiczne (toczeń rumieniowaty układowy, reumatoidalne zapalenie stawów, mieszana choroba tkanki łącznej)
- stwardnienie rozsiane
- amyloidoza (skrobiawica)
Najczęstsze wskazania do auto- i allotransplantacji
Wskazania do AUTO-HSCT
- ostra białaczka szpikowa
- ostra białaczka limfoblastyczna
- zespoły mielodysplastyczne
Wskazania do ALLO-HSCT
- szpiczak plazmocyowy
- chłoniaki niehodgkinowskie
- chłoniak Hodgkina
Transplantacja szpiku kostnego: przebieg
I etap - kondycjonowanie
Zabieg transplantacji szpiku rozpoczyna się od włączenia intensywnej terapii przeciwnowotworowej, która nazywana jest kondycjonowaniem. Ma ona na celu zniszczenie nie tylko komórek nowotworowych, ale także limfocytów biorcy szpiku, które mogłyby spowodować odrzucenie przeszczepu.
Kondycjonowanie polega na podawaniu biorcy tak dużych dawek chemioterapeutyków lub skojarzonej chemioterapii z radioterapią, aby wywołać nieodwracalne zniszczenie szpiku kostnego. Jest to leczenie mieloablacyjne.
Do głównych powikłań tej terapii należą:
- obniżenie odporności i podatność na wszelkie infekcje
- nudności
- wymioty
- zapalenie śluzówek przewodu pokarmowego
- pojawianie się krwawych wylewów
- utrata owłosienia
Ważne jest, aby poinformować pacjentów o możliwości zdeponowania spermy w banku spermy i zamrożenia komórek jajowych, ponieważ tak intensywna terapia może spowodować utratę lub znaczne obniżenie płodności.
II etap - wszczepienie
Pobrane od dawcy komórki macierzyste przeszczepia się biorcy w postaci centralnej infuzji dożylnej, czyli korzystając z założonego w warunkach bloku operacyjnego wkłucia do jednej z żył centralnych.
III etap - wczesny okres poprzetoczeniowy
Typową cechą dla wczesnego okresu poprzetoczeniowego jest występowanie pancytopenii, czyli obniżenie ilości wszystkich elementów morfotycznych krwi - erytrocytów, płytek krwi oraz leukocytów.
IV etap - regeneracja szpiku kostnego
Transplantacja (przeszczep) szpiku kostnego: powikłania
Choroba przeszczep przeciwko gospodarzowi (GvHD, ang. graft versus host disease)
- ostra choroba przeszczep przeciwko gospodarzowi (aGvHD, ang. acute GvHD)
Ostra choroba przeszczep przeciwko gospodarzowi występuje w ciągu 100 dni po przeszczepieniu. Wynika z ataku limfocytów T dawcy, czyli komórek układu odpornościowego, skierowanym przeciwko tkankom biorcy.
Ostra choroba GvHD może ustępować lub przechodzić w postać przewlekłą. Warto wspomnieć, że jest to główna przyczyna śmiertelności potransplantacyjnej!
Mimo doboru dawców zgodnych w układzie HLA, może pojawić się GvHD i wczesne odrzucenie przeszczepu, ponieważ istnieje wiele innych determinant antygenowych kodowanych na innych chromosomach, które nie są rutynowo badane.
aGVHD to reakcja względnie często występująca, obserwowana u około 40-70% pacjentów, dlatego tak ważne jest aby często kontrolować stan chorych poddawanych zabiegowi.
Opisano 3 charakterystyczne objawy, typowe dla wczesnej reakcji GvHD:
- zmiany skórne, jak zaczerwienienie, pęcherze, uogólniona erytrodermia
- zaburzenia funkcji wątroby, obserwowane początkowo jedynie w postaci nieprawidłowych wyników badań laboratoryjnych (podwyższona aktywność fosfatazy alkalicznej i stężenia bilirubiny)
- wodnista biegunka
Zapobieganie ostrej reakcji przeszczep przeciwko gospodarzowi polega głównie na właściwym doborze dawcy tkanki w układzie HLA.
- przewlekła (cGvHD, ang. chronic GvHD)
Przewlekła choroba przeszczep przeciwko gospodarzowi występuje powyżej 100. dnia po przeszczepieniu krwiotwórczych komórek macierzystych. Występuje ona u ok.33% biorców przeszczepów allogenicznych od dawców spokrewnionych, nie występuje natomiast u biorców przeszczepów autogenicznych.
Za wykształcenie tej reakcji u biorców odpowiadają limfocyty T dawcy, które rozpoznają tkanki biorcy jako obce i je niszczą.
Przewlekła choroba GvHD obejmuje wiele narządów, obserwuje się objawy w postaci zmian skórnych i błon śluzowych, schorzeń narządu wzroku, wątroby, płuc, a także patologii w obrębie przewodu pokarmowego.
Warto wspomnieć, że śmiertelność w przebiegu przewlekłej GvHD jest znacznie niższa niż w przebiegu ostrej GvHD. Wyróżnia się ograniczoną i uogólnioną postać przewlekłej choroby przeszczep przeciw gospodarzowi.
- Klasyfikacja przewlekłej choroby przeszczep przeciw biorcy
|
Ograniczona przewlekła GvHD (jedno kryterium lub oba) |
Zajęcie skóry ograniczoneDysfunkcja wątroby z powodu cGvHD |
| Uogólniona przewlekła GvHD |
Uogólnione zajęcie skóry lubOgraniczone zajęcie skóry i/lub dysfunkcja wątroby z powodu cGvHD orazHistopatologia wątroby wskazuje na przewlekłe agresywne zapalenie wątroby, martwicę lub marskość wątrobylubZajęcie oczu (test Schirmera <5mm) lubZajęcie mniejszych gruczołów ślinowych lub błony śluzowej w biopsji wargi lubZajęcie jakiegokolwiek organu docelowego |
Choroba przeszczep przeciwko białaczce (GvL, ang. graft versus leukemia)
Reakcja przeszczep przeciwko białaczce obserwowana jest u biorców przeszczepów allogenicznych, czyli sytuacji w której krwiotwórcze komórki macierzyste pochodzą od dawców spokrewnionych bądź nie.
Występuje ona dzięki wprowadzeniu do organizmu biorcy komórek układu odpornościowego dawcy, limfocytów T i komórek NK, które rozpoznają i niszczą pozostałe w organizmie biorcy komórki nowotworowe.
Zapalenie błon śluzowych
Zapalenie błon śluzowych przewodu pokarmowego jest najczęstszym powikłaniem obserwowanym u pacjentów poddawanych transplantacji szpiku, której przyczyną jest stosowanie intensywnej chemioterapii przed zabiegiem.
Głównymi objawami są mnogie afty w jamie ustnej, nudności, bolesne skurcze brzucha i biegunka. Z powodu silnego bólu podczas połykania, niezbędne jest włączenie żywienia parenteralnego.
Ciężka pancytopenia
U chorych poddanych przeszczepowi szpiku często opisuje się zmniejszoną ilość wszystkich elementów morfotycznych krwi obwodowej, tzn. erytrocytów, leukocytów i płytek krwi. Skutkować to może wystąpieniem:
- ciężkiej, zagrażającej życiu niedokrwistości wymagającej przetaczania KKCz (koncentratu krwinek czerwonych)
- zaburzeń krzepnięcia krwi, objawiających się zależnie od stopnia małopłytkowości: wybroczynami, wylewami krwawymi, krwawieniem z nosa czy uszu
- ciężkich infekcji bakteryjnych, grzybiczych, czy wirusowych, wymagających włączenia odpowiednio antybiotykoterapii, leków przeciwgrzybiczych lub leków przeciwwirusowych
Infekcje
W związku z obniżeniem odporności u osób po zabiegu przeszczepienia komórek macierzystych szpiku stwierdza się wyższą podatność na infekcje bakteryjne, wirusowe, a także zakażenia grzybicze. Do patogenów najczęściej wykrywanych u biorców zalicza się:
- bakterie: pneumokoki, Hemophilus influenzae
- wirusy: wirus cytomegalii, wirusy z grupy Herpes
- grzyby: Candida, Aspergillus, Pneumocystis carinii
Odrzucenie przeszczepianego szpiku kostnego
Odrzucenie przeszczepianego szpiku kostnego jest ciężkim powikłaniem obserwowanym u biorców poddawanych transplantacji allogenicznej, nie występuje w przypadku biorców przeszczepów autogenicznych (własnego szpiku pobranego przed intensywnym leczeniem).
Jest to sytuacja w której przeszczepione krwiotwórcze komórki macierzyste nie zaczynają proliferować i się różnicować, czyli nie rozpoczyna się proces hematopoezy.
Rokowanie pacjentów poddanych transplantacji
W literaturze opisywano występowanie nawrotów choroby u biorców przeszczepów autogenicznych znacznie częściej niż u biorców przeszczepów allogenicznych. Prawdopodobnie wynika to z faktu, iż w przypadku przeszczepu własnego szpiku kostnego nie obserwowano reakcji przeszczep przeciwko białaczce, której wykształcenie jest bardzo korzystne.
Porady eksperta

![Stan przedcukrzycowy dotyczy nawet 5 mln Polaków. Ciebie też? Sprawdź to [TEST]](https://cdn.galleries.smcloud.net/t/galleries/gf-TRZ7-kaJ1-ptSh_cukrzyca-pomiar-cukru-320x213.jpg)































